 |
Координационное число 6 и выше
|
|
|
|
Для КЧ 6 характерно октаэдрическое расположение лигандов, что отвечает sp 3 d 2- или d 2 sp 3 -гибридизации АО комплексообразователя: 
Октаэдрическим строением обладают ионы [PtCl6]2-, [Fe(CN)]6]3-, [Al(H2O)2(OH)4]-, [SnCl6]2-, [Co(NO2)6]3- и многие другие. Октаэдрическое строение комплексов с КЧ 6 является наиболее энергетически выгодным.
Геометрия комплексов с КЧ 7 отвечает пентагональной бипирамиде (sp 3 d 3 -гибридизация). Если КЧ принимает большее значение, то конфигурация комплекса сильно усложняется, причем возможно существование нескольких координационных многогранников, взаимно превращающихся друг в друга.
Глава 4. Изомерия комплексных соединений
С 15. Под изомерией понимают способность веществ образовывать несколько соединений одинакового состава, отличающихся взаимным расположением атомов в молекуле, а следовательно, различных по свойствам.
У КС явление изомерии обусловлено:
· различиями в строении и координации лигандов
· различиями в строении внутренней координационной сферы
· разным распределением частиц между внутренней и внешней сферой.
Основные виды изомерии КС – геометрическая, оптическая, сольватная (или гидратная) и ионная.
Изомерия лигандов
С 16. Изомерия лигандов подразделяется на связевую (которая определяется разным типом координации одного и того же лиганда), и собственно изомерию лиганда.
Примерами связевой изомерии - существование нитро- и нитрито-комплексов кобальта(III) состава K3[Co(NO2)6] и K3[Co(ONO)6], в которых координация лиганда NO2- осуществляется через атом азота или атом кислорода.
Другой пример – координация тиоцианат-иона NCS- через атом азота или через атом серы, с образованием тиоцианато-N- или тиоцианато-S-комплексов.
|
|
|
Геометрическая изомерия
С 17. Геометрическая изомерия вызвана неодинаковым размещением лигандов во внутренней сфере относительно друг друга. Необходимым условием геометрической изомерии является наличие во внутренней координационной сфере не менее двух различных лигандов. Геометрическая изомерия проявляется преимущественно у КС, имеющих октаэдрическое строение, строение плоского квадрата или квадратной пирамиды.
КС с тетраэдрическим, треугольным и линейным строением геометрических изомеров не имеют, т.к. места расположения лигандов двух разных видов вокруг ЦА равноценны.



С 18. Комплексы, имеющие строение плоского квадрата, при наличии двух разных лигандов L¢ и L² уже могут иметь два изомера (цис- и транс-):

Примером комплексного соединения, имеющего цис - и транс -изомеры, может служить дихлородиамминплатина(II):

КС состава [ML¢3L²] со структурой плоского квадрата не может иметь изомеров: положение лиганда L²равновероятно в любом углу квадрата. Когда же появляется два разных лиганда, то уже возможно существование двух изомеров (цис - и транс -), отличающихся по свойствам. Так, цис -дихлородиамминплатина(II) – оранжево-желтые кристаллы, хорошо растворимые в воде, а транс -дихлородиамминплатина(II) – кристаллы бледно-желтого цвета, растворимость которых в воде несколько ниже, чем у цис -изомера.
С 19. Октаэдрические комплексы могут иметь множество изомеров. Если в комплексном соединении такого рода все шесть лигандов одинаковы ([ML6]) или отличается от всех остальных только один ([ML¢5L²]), то возможность различного расположения лигандов по отношению друг к другу отсутствует. Например, у октаэдрических соединений [ML¢5L²] любое положение лиганда L² по отношению к остальным пяти лигандам L¢ будет равноценным и поэтому изомеров здесь не должно быть:

Появление двух лигандов L² в октаэдрических комплексных соединениях приведет к возможности существования двух геометрических изомеров. В этом случае появляются два различных способа расположения лигандов L² друг относительно друга. Например, катиондигидроксотетраамминкобальта(III) [Co(NH3)4(OH)2]+ имеет два изомера:
 <
<
|
|
|
Оптическая изомерия
С 20. Оптическая изомерия связана со способностью некоторых комплексных соединений существовать в виде двух форм, не совмещаемых в трехмерном пространстве и являющихся зеркальным отображением друг друга, как левая рука и правая. Поэтому оптическую изомерию называют иногда еще зеркальной изомерией.
Темно-зеленые кристаллы тригидрата триоксалатокобальтата(III) аммония (NH4)3[Co(ox)3]. 3 H2O существуют в виде двух оптических изомеров, комплексный анион которых имеет октаэдрическое строение. Т.к. полное изображение бидентатного оксалатного лиганда неудобно, его обозначают в виде дуги, соединяющей вершины октаэдра:
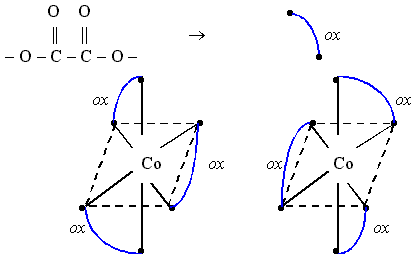
Расположение лигандов в оптических изомерах комплексного аниона [Co(ox)3]3- таково, что анионы соотносятся между собой как предмет и его зеркальное изображение.
С 21.Оптические изомеры отличаются тем, что их растворы способны вращать плоскость поляризации светового луча.
|
|
|


