 |
4. Второй класс ферментов и реакции, которые они катализируют.
|
|
|
|
4. Второй класс ферментов и реакции, которые они катализируют.
Согласно международной классификации и номенклатуре ко 2 классу ферментов относятся трансферазы.
К классу трансфераз относят ферменты, катализирующие
реакции межмолекулярного переноса различных атомов, групп атомов
и радикалов. Наименование их составляется по форме «донор: транспор-
тируемая группа – трансфераза».
Различают трансферазы, катализирующие перенос одноуглеродных ос-
татков, ацильных, гликозильных, альдегидных или кетонных, нуклеотидных остатков, азотистых групп, остатков фосфорной и серной кислот и др.
Например: метил- и формилтрансферазы, ацетилтрансферазы, амино-
трансферазы, фосфотрансферазы и др.
A—X + B ↔ A + B—X.
В зависимости от характера переносимых групп выделяют:
1)Фосфотрансферазы - это ферменты, катализирующие перенос остатка фосфорной кислоты.
2)Аминотрансферазы ускоряют перенос аминогруппы.
3)Гликозилтрансферазы ускоряют реакции переноса гликозильных остатков,
4)Ацилтрансферазы катализируют процессы переноса ацилов (радикалов карбоновых кислот) на спирты, амины, аминокислоты и другие соединения.
и др.
5. Что является конечным акцептором электронов и протонов, переносимых от окисляемых веществ?
Конечным акцептором электронов в дыхательной цепи является кислород.
билет 6:
1. Факторы влияющие на активность ферментов,
1)Температура. Скорость ферментативной реакции увеличивается в 1, 5-2 раза при повышении температуры на 10оС. Однако, этот процесс не беспределен, т. к. при t выше 40оС присоединяются явления тепловой денатурации, и активность фермента стремительно падает. Максимальную скорость ферментативные реакции имеют при температуе тела, т. е. при 37-38о С. При низких температурах активность ферментов также снижается, но они не разрушаются.
|
|
|
2)Влияние рН. Каждый фермент проявляет свое действие в определенных, довольно узких пределах значений рН. Оптимум рН - это. такое значение рН, при котором активность фермента будет максимальной. Ферменты, как белковые молекулы являются полиэлектролитами, и их заряд зависит от рН. Так, пепсин - фермент, расщепляющий белки в желудке, имеет оптимум рН около 1, 5. Ферменты, расщепляющие белки в кишечнике, имеют оптимум рН 8-9
3)Присутствие активаторов и ингибиторов. Активность ферментов зависит от наличия в реакционной среде различных соединений. Вещества, которые повышают каталитическую активность ферментов, называются активаторами. В качестве активаторов могут выступать ионы металлов (натрия, калия, магния, кальция, цинка, меди, марганца, железа) и другие вещества (ионы йода, брома, хлора, SH-группы).
Ингибиторы - подавляют действие ферментов. Они могут быть общими и специфическими. Общие – это те, которые инактивируют действие всех ферментов. К ним относятся соли тяжелых металлов (свинца, серебра, ртути), трихлоруксусная кислота (ТХУ), танин. Специфические - действуют только на определенную группу ферментов. Для ферментов дыхания и брожения ингибиторами являются галогенсодержащие соединения (хлорацетфенол, йодацетамид и т. д. ).
4)Концентрация субстрата и фермента.
Скорость большинства ферментативных реакций прямо пропорциональна концентрации фермента (рис. 14) в реакционной смеси (концентрация субстрата при этом постоянна).
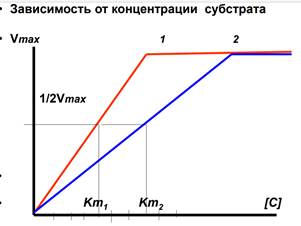
Vmax - максимальная скорость реакции.
Km - константа Михаэлиса.
Km - равна той концентрации субстрата, при которой измеренная скорость Vo равна половине Vmax.
Чем больше величина Кm, тем медленнее происходит «насыщение» фермента, т. е. тем меньше его сродство к субстрату
|
|
|
5) Изменение самого фермента, его структуры или его количества. Это связано с важнейшим свойством ферментов, его способностью к регулируемости.
2. 3 класс ферментов и реакции, которые они катализируют
В соответствии с международной Классификацией ферментов, по типу катализируемой реакции все ферменты подразделяются на 6 классов.
К 3му классу относят Гидролазы, которые катализируют гидролитическое расщепление сложноэфирных (эстеразы), пептидных (пептидгидролазы), гликозидных связей, связей С—N в амидах, амидинах и нитрилах, олиго- и полисахаридов, связи элемент-кислород в ангидридах.
3. формула кофермента дегидрогеназ, в состав которых входит витамин ниацин.
НАД - никотинамидадениндинуклеотид
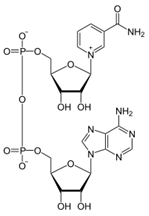
4. комплексы дыхательной цепи и где они локализованы,
Компонентами дыхательной цепи являются ферментные белки с относительно прочно связанными низкомолекулярными простетическими группами. Такие комплексы у эукариот локализуются во внутренней стороне мембраны митохондрий, а у прокариот – в плазматической мембране.
Компоненты дыхательной цепи погружены в двойной липидный слой. Речь идет о большом числе ферментов, коферментов и простетических групп, различных дегидрогеназ и транспортных систем, участвующих в переносе электронов и водорода. Белковые компоненты могут быть выделены из мембраны.
|
|
|


