|
Гарвардские критерии смерти головного мозга
|
|
|
|
Гарвардские критерии смерти головного мозга
Полное отсутствие словесного контакта и реакции на действие любого раздражителя
Никаких координированных и судорожных движений. Нет дыхательных движений, в том числе и его патологических ритмов
Полное угнетение всех рефлексов
Полное отсутствие какой-либо активности на электроэнцефалограмме (плоская электроэнцефалограмма)
Персистирующий вегетативный статус характеризуют стойкое угнетение когнитивных функций и потеря способности к высшей нервной деятельности. Наиболее частые причины статуса у больных - это острые инфекции, отравления, тяжелые механические травмы, кровопотеря и электротравма. Больной в персистирующем вегетативном статусе прикован к постели, он мочится и ходит под себя. При этом он не может питаться самостоятельно, и ему проводят исскусственное и нередко смешанное питание (энтеральное по назогастральному зонду и парентеральное). У таких пациентов обычно нет необходимости в интенсивной терапии, направленной на устранение расстройств внешнего дыхания и кровообращения. Это свидетельствует о достаточно сохраненной регуляции внешнего дыхания и кровообращения. В персистирующий вегетативный статус больные обычно переходят из состояния комы. При этом глаза открываются и создается впечатление пробуждения. Больные в статусе могут зевать, издавать нечленораздельные звуки, а также совершать беспорядочные, но частично координированные движения. Все это может сочетаться с признаками распространенного и необратимого поражения нейронов головного мозга (табл. 16. 1). Если за три месяца пациент не выходит из персистирующего вегетативного статуса, то восстановление когнитивных функций можно считать почти невозможным.
|
|
|
Глава 17
ДЫХАТЕЛЬНАЯ НЕДОСТАТОЧНОСТЬ И АРТЕРИАЛЬНАЯ ГИПОКСЕМИЯ
Основная функция системы внешнего дыхания - это поглощение из внешней среды кислорода и выведение в нее из внутренней среды углекислого газа.
Дыхательная недостаточность - это состояние организма вследствие неспособности системы внешнего дыхания обеспечить:
♦ поглощение легкими 02 и уровень его напряжения в артериальной крови (РаО2), достаточные для адекватного потребностям организма насыщения гемоглобина кислородом;
♦ выведение из организма углекислого газа, позволяющее организму удерживать концентрацию протонов во внеклеточной жидкости и плазме крови ([Н*]) в диапазоне нормальных изменений.
Кроме того, под дыхательной недостаточностью следует понимать неспособность системы внешнего дыханш реагировать ростом поглощения кислорода легкими и экскреции ими углекислого газа в ответ на увеличение потребности организма в кислороде (рост потребления организмом О2) и на возросшую потребность в экскреции углекислого газа (усиление высвобождения углекислого газа в ходе обмена веществ во внутреннюю среду организма).
Снижение в артериальной крови напряжения кислорода и рост в ней напряжения углекислого газа (РаС02) может быть следствием роста потребления кислорода организмом (П02) и образования в нем углекислого газа при физической нагрузке, лихорадке, сепсисе, при неспецифических компенсаторных процессах («стресс-реакция»), при тиреотоксикозе, а также при других патологических состояниях и приспособительных реакциях. При этом в определенные периоды болезни и патологического процесса напряжения газов в крови по мере снижения утилизации организмом свободной энергии возвращаются в «нормальные» пределы. Это не означает устранения терапией дыхательной недостаточности. Она остается скрытой, и проявляет себя артериальными гипоксемией и гиперкапнией при последующих по ходу болезни росте потребления кислорода и образования углекислого газа.
|
|
|
Легочный газообмен происходит на уровне терминальных респираторных единиц (ТРЕ) легких. ТРЕ (респирон) - это часть легких, дистальная по отношению к конечной нереспираторной бронхиоле, которая омывается смешанной венозной кровью, поступающей по ветви легочной артерии (легочной артериоле), параллельной данной терминальной нереспираторной бронхиоле. Легочная артериола распадается на капиллярную сеть, обволакивающую альвеолы и образующую легочные венулы, находящиеся на периферии ТРЕ. Такое строение ТРЕ в структурном отношении обеспечивает продвижение смешанной венозной крови строго из артериол через легочные капилляры в венулы и ее оксигенацию на уровне альвеол.
Дня наиболее полных на уровне одного респирона оксигенации смешанной венозной крови и освобождения ее от углекислого газа (легочный газообмен) необходимо наличие и совпадение во времени двух условий:
1. Достаточное поступление кислорода из внешней среды в состав альвеолярной газовой смеси, то есть определенный уровень минутной альвеолярной вентиляции (МАВ) дыхательной смесью газов с достаточным содержанием в ней кислорода. Кроме того, достаточная МАВ выступает необходимым условием адекватной экскреции углекислого газа в ходе внешнего дыхания из смешанной венозной крови и альвеолярной газовой смеси во внешнюю среду.
2. Оптимальное снабжение респирона смешанной венозной кровью.
Если на уровне одного респирона МАВ начинает преобладать над
кровотоком, то есть становится избыточной, то патогенных сдвигов в напряжении кислорода и углекислого газа в крови, которую содержат венулы данного респирона, не произойдет. Однако рост МАВ одних респиро- нов, одной совокупности структурно-функциональных единиц легких, приводит к падению вентиляции других, а значит и к нарушению в них легочного газообмена. Причиной нарушений газообмена в легких может быть и преобладание снабжения смешанной венозной кровью одних рес- пиронов за счет других.
|
|
|
Дыхательная недостаточность - это всегда следствие нарушений соответствия МАВ структурно-функциональных единиц легких, их отделов и частей, всех легких объемной скорости кровотока, то есть расстройств вентиляционно-перфузионных отношений.
В физиологических условиях всегда существует нормальная вариабельность вентиляционно-перфузионных отношений респиронов и отделов легких, которая на уровне всех легких не приводит к дыхательной недостаточности. При дыхательной недостаточности физиологическая вариабельность трансформируется в патологическую. В результате на уровне всей системы внешнего дыхания нарушается легочный газообмен. В силу большей диффузионной способности углекислого газа нарушения легочного газообмена чаще сначала приводят к патогенному падению оксигенации смешанной венозной крови, то есть обуславливают артериальную гипоксемию.
АРТЕРИАЛЬНАЯ ГИПОКСЕМИЯ
Под артериальной гипоксемией понимают патологически низкий уровень оксигенации смешанной венозной крови, в результате которого транспорт кислорода от легких на периферию становится таким низким, что возникает респираторная гипоксия.
Артериальная гипоксемия чаще всего выступает следствием:
♦ нарушений физиологической вариабельности вентиляционно-пер- фузионных отношений (ВПО) респиронов и отделов легких;
♦ патологического внутрилегочного шунтирования крови справа налево, то есть роста объема неоксигенированной смешанной венозной крови, который проходит через легкие в артериальную кровь, не участвуя в легочном газообмене;
♦ снижения парциального давления кислорода во вдыхаемой газовой смеси;
♦ падения напряжения кислорода в смешанной венозной крови (Ру02);
♦ нарушений диффузии газов через альвеоло-капиллярную мембрану;
♦ низкого МАВ, то есть гиповентиляции.
Степень тяжести артериальной гипоксемии оценивают в зависимости от уровня напряжения кислорода в артериальной крови (табл. 17. 1).
| Таблица 17. 1 Степени тяжести артериальной гипоксемии
|
ПАТОЛОГИЧЕСКИЕ ВАРИАБЕЛЬНОСТЬ ВЕНТИЛЯЦИОННО- ПЕРФУЗИОННЫХ ОТНОШЕНИЙ И ШУНТИРОВАНИЕ СМЕШАННОЙ ВЕНОЗНОЙ КРОВИ В ЛЕГКИХ КАК ПРИЧИНЫ АРТЕРИАЛЬНОЙ ГИПОКСЕМИИ
Общая площадь легочной мембраны, через которую происходит диффузия свободных молекул кислорода и углекислого газа, у здоровых людей колеблется от 160 до 200 м2. Эту площадь составляет сумма газообменной поверхности (легочной мембраны) около 100 000 респиронов (ТРЕ) и нескольких миллионов альвеол. Массоперенос кислорода и углекислого газа из альвеолярной газовой смеси в смешанную венозную кровь и в обратном направлении может быть достаточным лишь при условии незатрудненного кровоснабжения определенного числа оптимачьно вентилируемых респиронов. Общий объем крови, которую содержат легочные капилляры, составляет 100 мл. Этот объем крови «растягивается» до тончайшей пленки на поверхности легочной мембраны в пределах всех легких, что в структурно-функциональном отношении обеспечивает наиболее оптимальные условия для нормального легочного газообмена. Критериями соответствия легочного газообмена потребностям организма являются парциальные давления и напряжения газов в альвеолярной газовой смеси, артериальной и смешанной венозной крови (табл. 17. 2).
| Таблица 17. 2 Парциальные давления (напряжения) кислорода и углекислого газа в альвеолярной газовой смеси, смешанной венозной и артериальной крови в условиях относительного покоя у здорового молодого человека на уровне моря
|
Вентиляционно-перфузионное отношение (ВПО) на уровне всех легких представляет среднее значение ВПО их респиронов, участков легочной ткани и отделов легких. ВПО всех легких здорового человека в условиях относительного покоя равное 0, 8 может свидетельствовать о физиологической вариабельности ВПО в пределах всей легочной паренхимы. При физиологической вариабельности ВПО газообменный дыхательный коэффициенту отношение выделения углекислого газа к потреблению кислорода организмом (ПО2) равен метаболическому дыхательному коэффициенту, то есть отношению образования углекислого газа в ходе обмена веществ к П02, и они оба находятся на уровне близком 0, 8.
|
|
|
В легких здорового человека нет патологической вариабельности вен- тиляционно-перфузионных отношений респиронов, участков легочной паренхимы и отделов легких, несмотря на постоянное действие ряда факторов физиологической вариабельности ВПО:
♦ большее растяжение нижележащих и периферических отделов легких на высоте вдоха, обуславливающее преимущественное распределение дыхательного объема в эти участки легких;
♦ подверженность легочного кровотока влияниям со стороны силы земного притяжения, которые приводят к преобладанию кровоснабжения нижележащих респиронов;
♦ зависимость объемной скорости легочного кровотока в различных участках легких от величины дыхательного объема.
Тогда, когда в результате патологического процесса (пневмония, гемопневмоторакс, крайняя стадия респираторного дистресс-синдрома взрослых, ушиб легкого, раневой пульмонит и др. ) респироны легких в одинаковой степени теряют и альвеолы и легочные микрососуды, патологической вариабельности ВПО респиронов легких может и не развиться. При этом артериальной гипоксемии в условиях относительного покоя не возникает до тех пор, пока легкие не потеряют 70-80 % респиронов.
Если поступление смешанной венозной крови в какой-либо респирон или часть легких снижается или блокируется, то растет часть дыхательного объема, которая достигает альвеол, но не участвует в легочном газообмене. Это снижает поглощение кислорода всеми легкими, что вызывает падение напряжения кислорода в артериальной крови и артериальную ги- поксемию. Когда рост вентиляции части альвеол не сопровождается адекватным возрастанием кровотока по капиллярам, то из альвеолярной газовой смеси все легкие поглощают меньше кислорода. Это также увеличивает фракцию дыхательного объема, не задействованную для легочного газообмена, и снижает поглощение кислорода легкими. Результатом и того и другого варианта патологической вариабельности ВПО респиронов может быть артериальная гипоксемия. Если в легких одновременно возникают два описанных варианта нарушений ВПО, то на уровне всей системы внешнего дыхания это приводит к снижению физиологической площади легочной мембраны. Физиологическая площадь легочной мембраны - это та ее часть, диффузия через которую кислорода и углекислого газа приводит к полным, то есть ограниченным только градиентами парциальных давлений (напряжений), поглощению кислорода из альвеолярной газовой смеси, оксигенации смешанной венозной крови и ее освобождению от углекислого газа. Снижение физиологической площади легочной мембраны до определенного уровня приводит к артериальной гипоксемии.
Стеноз, обтурация легочной артерии или ее ветвей, а также множественная эмболия легочных микрососудов (диссеминированное внутрисо- судистое свертывание, жировая эмболия, тромбоз микросгустками перелитой крови, агрегатами активированных тромбоцитов и нейтрофилов при травматическом шоке и сепсисе) ведут к образованию альвеолярных мертвых пространств, то есть вентилируемых, но не омываемых смешанной венозной кровью альвеол. В результате возникает различие между РаС02 и парциальным давлением углекислого газа в конечной части выдыхаемого воздуха, которое считают эквивалентным парциальному давлению углекислого газа в альвеолярной газовой смеси, РАС02. Это результат полного прекращения в респиронах с только мертвыми альвеолярными пространствами переноса углекислого газа через легочную мембрану. Смешанная венозная кровь из таких респиронов по коллатера- лям устремляется в легочные венулы других ТРЕ, не отдав в альвеолярную газовую смесь углекислый газ. В результате возрастает шунтирование смешанной венозной крови в легких, что обуславливает:
♦ снижение различия между напряжением углекислого газа в смешанной венозной крови и РаС02;
♦ рост различия между РаС02 и РАС02.
Первоначально при синдроме распространенной микроэмболизации в легких компенсаторная гипервентиляция в ответ на рост РаС02 через увеличение экскреции углекислого газа предотвращает гиперкапнию, то есть патологически высокое РаС02. Если в результате обструкции легочных микрососудов поглощение кислорода легкими падает в такой степени, что возникает артериальная гипоксемия, то снижение кислородной емкости крови и падение в ней РаОг оказывают на сердце отрицательное инотропное действие. Падение сократимости сердца может привести к снижению минутного объема кровообращения (МОК).
Падение минутного объема кровообращения в данном случае происходит не только из-за артериальной гипоксемии. МОК снижается вследствие роста общего легочного сосудистого сопротивления как причины правожелудочковой сердечной недостаточности. Компенсаторная гипервентиляция в ответ на артериальную гипоксемию повышает ПОг, что ускоряет развитие циркуляторной гипоксии. Циркуляторная гипоксия при синдроме распространенной микроэмболизации в легких представляет собой результат легочной артериальной гипертензии, правожелудочковой сердечной недостаточности и связанного с ними падения МОК при высокой из-за повышенных энерготрат в системе внешнего дыхания потребности всего организма в кислороде.
Главными симтомами синдрома распространенной микроэмболизации в легких являются одышка и тахикардия, которые возникают и обостряются даже при минимальном увеличении физической нагрузки. Если при обследовании таких больных над легкими не слышат хрипов, рентгенологическое исследование не выявляет патологических изменений в легких, а анамнез не содержит данных, свидетельствующих о предшествующей явной или скрытой хронической сердечной недостаточности, то следует заподозрить распространенную эмболизацию микрососудов легких. Когда, кроме того, есть электрокардиографические признаки гипертрофии правого желудочка, то развитие синдрома сомнений вызывать не должно.
Распространенная микроэмболизация в легких - это не единственная причина возникновения в их паренхиме альвеолярных мертвых пространств. Причиной альвеолярных мертвых пространств служат патологические изменения легких при эмфиземе, которые через облитерацию микрососудов блокируют кровоснабжение респиронов.
Если вентиляция респирона полностью прекращается при сохраненном поступлении в него смешанной венозной крови (ВПО=0), то по вену- лам такого респирона начинает оттекать смешанная венозная кровь. Эта кровь проходит через легкие, не участвуя в легочном газообмене и составляя объем (величину) истинного патологического внутрилегочного шунтирования смешанной венозной крови.
Объем истинного патологического внутрилегочного шунтирования составляет та часть попавшей в легкие смешанной венозной крови, которая примешивается к артериальной, пройдя по капиллярам и венулам полностью невентилируемых респиронов.
Если вентиляция респиронов, участков и отделов легких, снижается без адекватного уменьшения в них объемной скорости кровотока, то легочный газообмен в них не прекращается, но продолжает оксигенироваться лишь часть поступившей в них смешанной венозной крови. Ос
тавшаяся часть составляет величину физиологического шунтирования, которая вместе с объемом истинного патологического внутрилегочного шунтирования составляет у больных величину патологического внутри- легочного шунтирования смешанной венозной крови.
Обструктивные расстройства альвеолярной вентиляции, вызывая ее неравномерность, резко увеличивают число респиронов, в которых из-за низкой относительно снабжения смешанной венозной кровью вентиляции происходит физиологическое шунтирование смешанной венозной крови. Таким образом формируется основное звено патогенеза артериальной ги- поксемии у больных с обструктивными расстройствами внешнего дыхания вследствие бронхиальной астмы и астматического статуса.
ОБСТРУКТИВНЫЕ И РЕСТРИКТИВНЫЕ РАССТРОЙСТВА
АЛЬВЕОЛЯРНОЙ ВЕНТИЛЯЦИИ
Потеря легкими нормальных респиронов снижает физиологическую площадь легочной мембраны и через утрату части сосудов из системы легочной артерии повышает общее легочное сосудистое сопротивление. В результате поглощение кислорода легкими ограничивается патологически низким верхним пределом. Такое нарушение альвеолярной вентиляции и легочного газообмена называют рестрикционным (рестрикцией). О рестрикционном (лат. геэ^юйо, ограничение) нарушении легочного газообмена может свидетельствовать частое и поверхностное дыхание.
Рестриктивные расстройства внешнего дыхания - это результат ограничения способности достижения системой внешнего дыхания своих конечных полезных приспособительных результатов из-за потери главным эффектором системы, легкими, определенного числа нормально функционирующих респиронов.
Сравнительно недавно одной из причин падения поглощения кислорода легкими считали альвеолярно-капиллярный блок, то есть снижение массопереноса кислорода в респиронах, связанное с утолщением легочной мембраны вследствие патологических процессов в интерстиции легких. Сейчас ясно, что в большинстве случаев хронических заболеваний с патологическими изменениями в легочном интерстиции падение поглощения кислорода легкими возникает как рестрикционное нарушение легочного газообмена.
Обструктивные расстройства внешнего дыхания (обструкция) (лат. оЬБ^исйо - преграда, помеха) связаны с аномальным возрастанием сопротивления продвижению смеси газов по дыхательным путям во время вдоха и (или) выдоха.
Выделяют стабильное обструктивное расстройство внешнего дыхания, которое выявляют как в фазу вдоха, так и в фазу выдоха. Стабильную обструкцию обуславливает постоянное сужение верхних дыхательных путей, связанное со злокачественными опухолями, пороками развития и последствиями ранений и травм соответствующей локализации. К стабильной обструкции приводит и постоянное патогенное сужение дыхательных путей небольшого диаметра при хроническом обструктивном бронхите и бронхиальной астме. Лабильное обструктивное расстройство внешнего дыхания преимущественно выражено или в фазу вдоха или во время выдоха, то есть может быть инспираторным или экспираторным. При параличе дыхательных связок или трахеомаляции на экстратора- кальном уровне обструкция в основном или исключительно возникает во время вдоха, являясь инспираторной. Экспираторная обструкция обычно происходит на интраторакальном уровне. Такую обструкцию вызывают: коллапс интраторакальной части трахеи из-за трахеомаляции, спадение бронхов и бронхиол небольшого диаметра вследствие патологических изменений легочного интерстиция при эмфиземе.
При бронхиальной астме и хроническом обструктивном бронхите просвет дыхательных путей небольшого диаметра (от сегментарных бронхов до терминальных нереспираторных бронхиол) постоянно сужен вследствие их закупорки секретом, бронхоспазма и отека слизистой оболочки. Это обуславливает как инспираторные, так и экспираторные об- структивные расстройства альвеолярной вентиляции. При этом в результате патологической динамической компрессии дыхательных путей (см. ниже) экспираторные обструктивные расстройства выражены в большей степени. Рост линейной скорости газотока в дыхательных путях небольшого диаметра из-за их сужения, патологическая динамическая компрессия таких дыхательных путей в фазу выдоха вызывают колебания выдыхаемой газовой смеси и стенок дыхательных путей, которые при аускультации воспринимаются как свистящие (в основном экспираторные) хрипы.
При нормальных регуляции функции внешнего дыхания и состоянии ее эффекторов существует верхний предел объемной скорости газотока выдыхаемой газовой смеси, выше которого скорость не растет, несмотря на увеличение силы сокращений дыхательных мышц. Верхний предел объемной скорости газотока при выдохе обусловлен динамической компрессией дыхательных путей
Для осуществления выдоха внутриальвеолярное давление должно возрасти от атмосферного, которое мы будем считать нулевым. Рост давления смеси газов в просвете альвеол происходит через увеличение давления в плевральной полости, а значит и в перибронхиальных пространствах легких. Статическое давление выдыхаемой газовой смеси снижается по мере ее продвижения по дыхательным путям. В результате во время выдоха снижается градиент давлений между интерстицием легких (пе- рибронхиальные пространства) и просветом дыхательных путей. Как только где-либо на интраторакальном уровне давление в паренхиме легких и в перибронхиальных пространствах начинает преобладать над статическим давлением газовой смеси в просвете дыхательных путей (градиент давлений становится положительным), то происходит сдавление (компрессия) дыхательных путей, если только его не предотвращает ригидность их стенки.
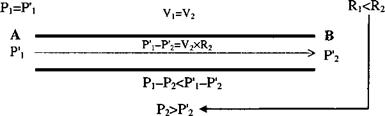
Градиент давлений между начальной (А) и конечной (В) точками определенного сегмента дыхательных путей находится в прямой связи с сопротивлением данного сегмента. Сужение просвета бронхиол и бронхов небольшого диаметра повышает сопротивление дыхательных путей данного уровня, увеличивает соответствующий градиент давлений и через падение статического давления выдыхаемой газовой смеси (Р2, Р'2, рис. 17. 1) может привести к спадению дыхательных путей.
| А........ В Р. -Р^У. хИ, Р]------------------------------------------------------------------------ > Р2
Рис. 17. 1. Снижение давления в просвете дыхательных путей, обусловленное ростом их сопротивления в результате сужения просвета (Р1-Р2 - градиент статических давлений в просвете дыхательных путей; Я - сопротивление дыхательных путей; V - объемная скорость продвижения вдыхаемой газовой смеси по дыхательным путям) |
Рост сопротивления дыхательных путей снижает объемную скорость газотока по дыхательным путям, но линейная скорость продвижения выдыхаемой газовой смеси по отдельным бронхиолам и бронхам растет вследствие сужения их просвета. В результате падает статическое давление газовой смеси в просвете дыхательных путей, что служит еще одним из механизмов их патологической динамической компрессии, связанной с патологическим ростом сопротивления дыхательных путей.
Патологическая динамическая компрессия дыхательных путей служит одной из причин легочной эмфиземы у больных с хроническими обструк- тивными заболеваниями легких. Эмфизема развивается через постоянную задержку части выдыхаемой газовой смеси в легких и перераздувание альвеол после полного спадения дыхательных путей в результате патологической динамической компрессии. При этом параллельно с развитием эмфиземы выявляют патологическое возрастание остаточного объема и функциональной остаточной емкости легких.
Патологическая динамическая компрессия дыхательных путей еще в большей степени усиливает их сопротивление, что резко повышает использование свободной энергии для внешнего дыхания и потребление кислорода дыхательными мышцами. Рост потребления кислорода для внеш
него дыхания повышает потребление кислорода всем организмом (П02). Если при этом нет адекватного возрастания поглощения кислорода легкими, то возникает артериальная гипоксемия. При обструктивных расстройствах альвеолярной вентиляции не происходит достаточного для предотвращения артериальной гипоксемии роста поглощения кислорода легкими из-за обусловленной обструкцией патологической вариабельности вентиляционно-перфузионных отношений респиронов, участков и отделов легких.
Представим две идентичные по всем функциональным характеристикам структурно-функциональные единицы легких, в которые дыхательная смесь газов поступает по одному бронху (бронхиоле) (рис. 17. 2). Из этого бронха дыхательная смесь идет в структурно-функциональные единицы легких по их бронхам (бронхиолам) с одинаковым сопротивлением. Патогенное сужение просвета дыхательных путей структурно-функцио- нальных единиц легких происходит неравномерно, то есть происходит асинхронное реагирование структурно-функциональных единиц эффектора функций.

| ||||||
| ||||||
| ||||||
Известно, что при ламинарном характере газотока, который характеризует продвижение смеси газов по дыхательным путям небольшого диаметра, снижение радиуса их просвета в два раза увеличивает их сопротивление в 16 раз. Предположим, что в соответствии с принципом аси- хроннного реагирования после патогенной бронхоконстрикции (сужения просвета) радиус просвета бронхиолы одной структурно-функциональной единицы составляет 90 % радиуса другой. При ламинарном газотоке сопротивление - это обратная функция четвертой степени радиуса. Поэтому такое небольшое различие в радиусах приводит к значительному различию в сопротивлениях, при котором сопротивление бронхиолы одной
структурно-функциональной единицы больше сопротивления другой примерно в полтора раза. При турбулентном газотоке в более крупных по диаметру дыхательных путях небольшие различия в радиусе просвета также обуславливают значительные различия в сопротивлениях.
Разные сопротивления бронхиол приводят к разной объемной скорости тока по ним смеси газов. Время вдоха ограничено. Поэтому часть структурно-функциональных единиц с более низким сопротивлением дыхательных путей заполняется вдыхаемой газовой смесью избыточно, тогда, когда в другие, с высоким сопротивлением, она поступает недостаточно. Это приведет к снижению в конце фазы вдоха в части альвеол легких общего давления газовой смеси и парциального давления кислорода. Снижение РАОг через действие механизма алъвеоло-капиллярного рефлекса (спазм микрососудов прекапиллярного уровня респирона в ответ на падение парциального давления кислорода в альвеолярной газовой смеси) ограничивает снабжение смешанной венозной кровью респиронов, вентиляция которых снижена. Тем не менее, альвеоло-капиллярный рефлекс не может предотвратить снижения физиологической площади легочной мембраны, вызванного неравномерностью альвеолярной вентиляции вследствие ее обструктивных расстройств. Из-за гиповентиляции части респиронов возрастает шунтирование смешанной венозной крови, и возникает артериальная гипоксемия.
Обструктивные расстройства альвеолярной вентиляции при хроническом обструктивном бронхите и бронхиальной астме через увеличение сопротивления дыхательных путей снижают объемную скорость газотока по дыхательным путям в фазу выдоха. Рост сопротивления дыхательных путей приводит к снижению максимальной объемной скорости газотока при выдохе (пиковая скорость), которая у больных бронхиальной астмой находится на уровне меньшем, чем 60 л/мин, что может служить показанием к госпитализации. Падение объемной скорости газотока снижает объем газовой смеси, выдыхаемой при форсированном выдохе за его первую секунду (объем форсированного выдоха за первую секунду, ОФВО. Одновременно, но в меньшей степени, вследствие патологической динамической компрессии дыхательных путей у больного снижается объем максимально возможного и быстрого форсированного выдоха (форсированная жизненная емкость легких, ФЖЕЛ). Это приводит к снижению экспираторного индекса Тиффно, то есть отношения ОФВ1/ФЖЕЛ, до значений меньших, чем 75 %.
Крайняя степень обструктивных расстройств внешнего дыхания - это полная обтурация (закупорка) крупного бронха с прекращением вентиляции респиронов отдела легких. При этом альвеоло-капиллярный рефлекс не прекращает полностью поступление в невентилируемые респироны смешанной венозной крови. В результате кислород из состава альвеолярной газовой смеси уходит в смешанную венозную кровь, альвеолы спадаются, и развивается ателектаз. Истинное патологическое шунтирование смешанной венозной крови в легких при соответствующей распространенности ателектаза может быть причиной артериальной гипоксемии.
НЕДОСТАТОЧНАЯ ВЕНТИЛЯЦИЯ РЕСПИРОНОВ
КАК ПРИЧИНА АРТЕРИАЛЬНОЙ ГИПОКСЕМИИ
Гиповентшяцш - это состояние легочного газообмена, которое характеризуют артериальная гипоксемия и рост в артериальной крови напряжения углекислого газа вследствие несоответствия патологически низкой альвеолярной вентиляции объемной скорости тока оксигенируемой смешанной венозной крови
Артериальная гипоксемия вследствие гиповентиляции обусловлена не только падением парциального давления кислорода в альвеолах, вызванного тем, что кислород уходит из необновляемой альвеолярной газовой смеси в смешанную венозную кровь. Одновременно в альвеолах растет парциальное давление углекислого газа, что служит еще одним фактором снижения парциального давления 02 в альвеолярной газовой смеси.
Если нет патологических изменений легких и дыхательных путей, то гиповентиляция является следствием: нарушений центральной регуляции внешнего дыхания, паралича или слабости дыхательных мышц (диафрагмы в особенности). Дыхательная недостаточность при закрытой травме груди отчасти обусловлена нарушением целостности каркаса грудной клетки и пневмотораксом. Причины гиповентиляции почти эквивалентны причинам респираторного ацидоза.
Рестриктивные расстройства внешнего дыхания при респираторном дистресс-синдроме взрослых и тяжелой пневмонии, снижая физиологическую площадь легочной мембраны, вызывают респираторный ацидоз и гиповентиляцию как причину артериальной гипоксемии. Физиологическая площадь легочной мембраны может быть снижена в результате аспирации воды при утоплении. Аспирация кислого желудочного содержимого после регургитации вызывает синдром Мендельсона, патогенез которого составляет острое воспаление в ответ на первичную альтерацию вследствие высокого содержания протонов в альвеолах, интерстиции и клетках респиронов.
Асцит и ожирение снижают дыхательный объем и нарушают равномерность альвеолярной вентиляции. В результате растет часть респиронов с вентиляцией, низкой относительно объемной скорости кровотока. Ожирение предрасполагает к падению физиологической площади легочной мембраны после полостных оперативных вмешательств не только через низкую податливость грудной клетки, но и являясь фактором риска ателектазов в послеоперационном периоде.
Угнетение активности нейронов дыхательного центра как причину гиповентиляции обуславливают:
♦ побочные эффекты лекарственных средств;
♦ черепно-мозговые ранения и травмы с эпидуральной и (или) субду- ральной гематомой;
♦ злокачественные опухоли или их метастазы соответствующей локализации;
♦ абсцессы мозга и менингит;
♦ расстройства мозгового кровообращения и их следствия, инфаркт головного мозга и субарахноидальное кровоизлияние.
Причиной гиповентиляции могут быть нарушения сократительной способности дыхательных мышц в результате патологических изменений миоцитов или нарушений регуляции на уровне нейромышечного синапса. Способность миоцитов произвольных мышц к сокращению падает при таких заболеваниях как периодический паралич, а также вследствие выраженных гипокалиемии и гипофосфатемии. Ареактив- ность скелетных мышц к эфферентации на уровне синапса обуславливают миастения и такое заболевание как синдром Гийена-Барре. Кроме того, проведение нервного импульса через синапс к миоцитам блокируют лекарственные средства: миорелаксанты, антибиотики из группы аминогликозидов и др.
Наиболее частые в клинической практике причины низкого парциального давления кислорода во вдыхаемой газовой смеси, вызывающего артериальную гипоксемию, - это дефекты проведения искусственной вентиляции легких.
В остром периоде тяжелой раневой болезни циркуляторная гипоксия приводит к падению напряжения кислорода в смешанной венозной крови. Одновременно в легких может расти общий объем ее. Повышенное примешивание к артериальной крови смешанной венозной, напряжение кислорода в которой находится на патологически низком уровне, служит одной из причин артериальной гипоксемии после тяжелых ранений и травм.