 |
Представители класса, их применение.
|
|
|
|
Ацетилен – газ, без цвета и запаха со слабым наркотическим действием. Используется для сварки металлов, для получения каучуков: хлоропреновый, бутадиеновый.
Ацетилен является исходным продуктом для многих важнейших химических производств. Например, из ацетилена получают различные галогенопроизводные, такие как тетрахлорэтан СНCl2 – СНCl2 и трихлорэтилен СНCl = СCl2, являющиеся хорошими растворителями, а также винилхлорид
СН2 = СНCl, служащий мономером для получения поливинилхлорида.
Продукт присоединения воды к ацетилену – уксусный альдегид – и получаемая из него уксусная кислота широко используются в ряде промышленных синтезов.
13.Строение ацетилена. Образование сигма и П-связей. Химические свойства алкинов (реакции присоединения, окисления, восстановления, кислотные свойства).
Строение тройной связи.
Тройная связь представляет собой комбинацию одной -связи и двух -связей. Атомы углерода, связанные тройной связью, находятся в состоянии sp-гибридизации. Каждый атом имеет две sp-гибридные орбитали, расположенные под углом 180. За счёт осевого перекрывания орбиталей образуется -связь (рис.1), за счёт бокового перекрывания орбиталей образуются две -связи.
Оставшиеся негибридизированными рy- и pz- орбитали каждого атома углерода расположены под углом 90º одна к другой. При боковом перекрывании этих орбиталей с соответствующими р-орбиталями другого sp-гибридизированного атома углерода образуются две π-связи, расположенные в двух взаимно перпендикулярных плоскостях (рис.2).
Таким образом, тройная связь образуется из трёх пар обобществлённых электронов, т. е. это шестиэлектронная связь.
|
|
|
Отличительная черта тройной связи – высокая насыщенность электронами межатомного пространства, что приводит к стягиванию положительно заряженных ядер и сближению атомов углерода.
Длина тройной связи 0,120 нм, энергия 828 кДж/моль.
Химические свойства.
I. Реакции электрофильного присоединения (АЕ).
Химические свойства алкинов определяются наличием в их молекулах тройной связи.
π-электронная плотность тройной связи является объектом атаки электрофильной частицей и поэтому алкины склонны к реакциям электрофильного присоединения
Гидрирование.

Галогенирование.
Обесцвечивание бромной воды – качественная реакция для обнаружения тройной связи.
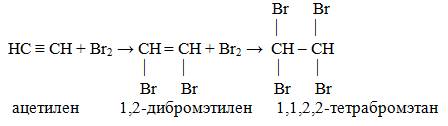
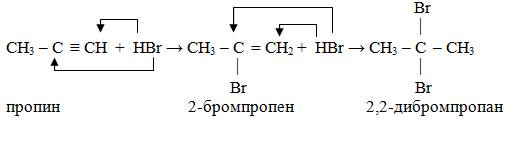
Гидрогалогенирование.
Алкины присоединяют последовательно две молекулы галогеноводорода. Сначала образуется моногалогензамещённый алкен, а затем дигалогензамещённый алкан. Присоединение идёт по правилу замещения Марковникова: атом водорода присоединяется к более гидрогенизированному атому углерода. В результате получаются дигалогеналканы, у которых оба атома галогена находятся при одном и том же атоме углерода.
Реакция гидратации.
Это одна из важнейших реакций алкинов, в результате которой получаются карбонильные соединения. Реакция гидратации алкинов была открыта русским химиком М. Г. Кучеровым (1881) и носит его имя.
Гидратация алкинов протекает в присутствии катализаторов – серной кислоты и сульфата ртути (II) HgSO4. На первой стадии реакции в результате присоединения молекулы воды образуется непредельный спирт, у которого гидроксильная группа находится непосредственно у атома углерода при двойной связи. Такие спирты принято называть виниловыми.
Отличительной чертой алифатических ненасыщенных соединений, содержащих гидроксильную группу при двойной связи, является их неустойчивость. В момент образования ониизомеризуются в более стабильные карбонильные соединения (альдегиды или кетоны). Эта закономерность носит название правила Эльтекова, по имени русского химика А. П. Эльтекова (1887).
|
|
|
Изомеризация состоит в том, что протон гидроксильной группы переходит к соседнему атому углерода при двойной связи с разрывом π-связи между атомами углерода и образованием её между атомами углерода и кислорода. Первый член гомологического ряда алкинов – ацетилен – превращается в результате этой реакции в уксусный альдегид.

II. Реакция окисления.
Алкины легко окисляются различными окислителями, в частности перманганатом калия. При этом раствор перманганата калия обесцвечивается, что служит указанием на наличие тройной связи. При окислении обычно происходит расщепление тройной связи и образуются карбоновые кислоты.

Обесцвечивание раствора KMnO4 – качественная реакция на тройную связь.
|
|
|


