|
7.5. Теплоемкость. Универсальная газовая постоянная R численно равна работе, которую совершает 1 моль идеального газа при изобарном расширении в процессе нагревания на 1 К.
|
|
|
|
7. 5. Теплоемкость
Количество теплоты, необходимое для нагревания системы на 1 К, называется теплоемкостью
С = 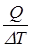 . (7. 11)
. (7. 11)
Теплоемкость единицы массы системы называют удельной теплоемкостью
c = 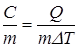 , (7. 12)
, (7. 12)
где Q - количество теплоты, сообщенное системе массой m, DT = Т2 - Т1 - изменение температуры системы.
Молярной теплоемкостью Сm называют теплоемкость одного моля вещества
Сm = 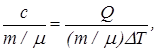 (7. 13)
(7. 13)
где m - молярная масса.
Количество теплоты, необходимое для нагревания вещества, рассчитывают по формуле
Q = CDT = mcDT = 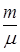 CmDT.
CmDT.
Теплоемкость вещества зависит от условий нагревания. Теплоемкость газа или жидкости при изобарном процессе (p = const) называют изобарной теплоемкостью Ср, а при изохорном процессе (V = const) - изохорной теплоемкостью СV. Всегда выполняется условие Ср > СV.
Для вещества в твердом состоянии Ср и СV незначительно отличаются друг от друга.
Молярная изохорная теплоемкость идеального газа СV = iR/2.
При изотермическом процессе (Т = const) количество теплоты, сообщенное газу, полностью идет на работу против внешнего давления, внутренняя энергия при этом не меняется, DU = 0, Q = A.
Теплоемкость при изотермическом процессе СТ = 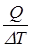 ® ¥.
® ¥.
При изобарном процессе (p = const) количество теплоты Q, подводимое к газу, расходуется на увеличение внутренней энергии DU и на совершение работы против внешних сил Q = DU + pDV.
Молярная изобарная теплоемкость идеального газа СР =  .
.
Разность молярных изобарной и изохорной теплоемкостей идеального газа равна универсальной газовой постоянной: СР - СV = R - (уравнение Майера).
Универсальная газовая постоянная R численно равна работе, которую совершает 1 моль идеального газа при изобарном расширении в процессе нагревания на 1 К.
|
|
|
7. 6. Адиабатный процесс
Термодинамический процесс, происходящий без теплообмена с окружающей средой, называется адиабатным.
Адиабатный процесс возможен в следующих случаях:
|
Рис. 7. 5 |
- теплопроводность оболочки равна нулю,
- процесс быстротекущий, и не успевает произойти теплообмен с окружающей средой,
- охвачены процессом очень большие объемы.
При адиабатном процессе первый закон термодинамики принимает вид
DU + A = 0, А = - DU. (7. 14)
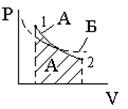
Поскольку внутренняя энергия идеального газа определяется температурой, то, следовательно, при адиабатном сжатии газа его температура увеличивается DТ > 0. При расширении газа работа совершается за счет убыли внутренней энергии газа, т. е. А > 0, DU < 0, что ведет к уменьшению его температуры DT < 0. Поэтому адиабата (А) круче изотермы (Б) (рис. 7. 5).
Адиабатная теплоемкость газа Сад = 0.
Равновесный адиабатный процесс описывается уравнением Пуассона
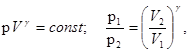 (7. 15)
(7. 15)
где g = СP/CV, g = (i + 2)/2 - показатель адиабаты.
Работа, совершаемая при адиабатном процессе, численно равна площади заштрихованной криволинейной трапеции (рис. 7. 5) и определяется выражением
 T1 - T2). (7. 16)
T1 - T2). (7. 16)
7. 7. Тепловые двигатели
|
Рис. 7. 6 |
Тепловым двигателем называется устройство, в котором происходит преобразование полученной в виде тепла энергии в механическую. К тепловым двигателям относятся паровые турбины, двигатели внутреннего сгорания (дизельные и карбюраторные), реактивные двигатели и т. п. Любой тепловой двигатель состоит из нагревателя, рабочего тела, холодильника (рис. 7. 6).
Тепловой двигатель получает тепло от источника, называемого нагревателем. В самом тепловом двигателе тепло поглощается телом, которое в результате нагревания совершает работу (приводит в движение поршень, вал турбины). Это тело называется рабочим телом (пар, продукты сгорания топлива). Отдача тепла является необходимым условием работы двигателя, т. е. не все тепло Q1, полученное от нагревателя, идет на совершение работы - часть его Q2 передается холодильнику. Механическая работа, совершенная тепловым двигателем А = Q1 - Q2.
|
|
|
|
Рис. 7. 7 |
В тепловых двигателях используются циклические (замкнутые) процессы (рис. 7. 7). На участке 1 - а - 2 рабочее тело получает тепло Q1 > 0 и расширяясь, совершает работу А1 > 0, на участке 2 - б - 1 рабочее тело сжимается, и над ним совершают работу внешние силы А2 < 0, при этом от рабочего тела передается тепло холодильнику Q2 < 0. Так как процесс циклический, то изменение внутренней энергии за цикл DU = 0.
Из первого начала термодинамики следует
Q1 + Q2 = A1 + A2.
Термическим коэффициентом полезного действия тепловой машины называется величина
 (7. 17)
(7. 17)
|
Рис. 7. 8 |
где А - работа, совершаемая машиной за цикл, численно равная площади цикла на графике в координатах (р, V) (рис. 7. 7), Q1 - количество теплоты, полученное от нагревателя за цикл, Q2 - количество теплоты, отдаваемое рабочим телом за цикл холодильнику.
Второе начало термодинамики устанавливает, что ни один тепловой двигатель не может работать без холодильника (Q2 ¹ 0), поэтому всегда h < 1. Максимальный к. п. д. имеет идеальная тепловая машина, работающая без трения с рабочим телом - идеальным газом, использующая цикл, состоящая из двух изотерм и двух адиабат (цикл Карно) (рис. 7. 8).
К. п. д. такой машины равен
 (7. 18)
(7. 18)
где Т1, Т2 - температуры нагревателя и холодильника соответственно.
Теплотворностью топлива (теплотой сгорания) называется величина, численно равная количеству теплоты, выделяемой 1 кг топлива или 1 м3 газа в нормальных условиях при полном сгорании
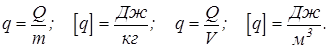
Отношение количества теплоты, переданное на нагревание тела, к количеству теплоты, выделяемой при сгорании топлива, называется коэффициентом полезного действия нагревателя

где с - удельная теплоемкость нагреваемого тела, m - его масса, DТ - изменение температуры тела при нагревании, mT - масса топлива.
|
|
|
|
|
|