 |
4.1. Молекулярно-кинетическая природа изменения температуры газа в процессе дросселирования
|
|
|
|
Как известно из общей термодинамики
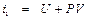 .
.
Тогда уравнение дросселирования (1. 4)
i2 = i1
можно записать в следующей форме:

или
 .
.
Как известно, в первом законе термодинамики для газового потока разность  называется работой проталкивания для 1 кг газа (по физическому смыслу это работа против внешних сил при перемещении 1 кг рабочего тела между сечениями потока 1 и 2).
называется работой проталкивания для 1 кг газа (по физическому смыслу это работа против внешних сил при перемещении 1 кг рабочего тела между сечениями потока 1 и 2).
Разность (U1 – U2) – это изменение удельной внутренней энергии при дросселировании.
Как известно из физики, внутренняя энергия – это сумма четырех составляющих:
− кинетическая энергия поступательного движения молекул;
− кинетическая энергия вращательного движения молекул;
− энергия внутримолекулярных колебаний;
− потенциальная энергия сил сцепления (притяжения) между молекулами.
Силы сцепления зависят от расстояния между молекулами, поэтому зависят от давления или объема, занимаемого газом. Таким образом, четвертая составляющая внутренней энергии зависит только от величины P или V.
Первые три составляющие U зависят только от температуры. У идеальных газов нет силы сцепления между молекулами, соответственно нет и четвертой составляющей U, поэтому внутренняя энергия идеального газа зависит только от первых трех ее составляющих, т. е. от температуры. Так как при дросселировании идеального газа Т1 = Т2, то U1 = U2 и P2V2 = P1V1.
У реальных газов при дросселировании потенциальная энергия сцепления между молекулами всегда растет, так как растет расстояние между молекулами из-за уменьшения давления (P2 < P1) и увеличения объема (V2 > V1).
В зависимости от области нахождения начальной точки дросселирования (Р1, Т1), одно и то же изменение давления приводит к различной величине возрастания объема. В связи с этим, соотношение между P1V1 и P2V2 также зависит от области начальных параметров дросселирования.
|
|
|
Для реальных газов возможны три варианта соотношения между P1V1 и P2V2:
1. P2V2 = P1V1, т. е. работа проталкивания равна нулю и, соответственно, U1 = U2. В этом случае внутренняя энергия не изменилась, но произошло перераспределение ее составляющих. Из-за уменьшения давления четвертая составляющая увеличилась, а кинетическая часть (первые три составляющие) на столько же уменьшилась. Уменьшение кинетической составляющей, определяющей температуру газа, вызвало уменьшение температуры газа при дросселировании.
2. P2V2 > P1V1, т. е. работа проталкивания больше нуля и, соответственно, U1 > U2. В этом случае, помимо обязательного перераспределения внутренней энергии в пользу потенциальной, произошло еще и снижение общего уровня U из-за расходования ее на совершение положительной работы проталкивания (по правилу знаков работа считается положительной, если она совершается системой). Понижение температуры газа при дросселировании в этом случае будет еще больше, нежели в первом случае.
3. P2V2 < P1V1, т. е. работа проталкивания меньше нуля и, соответственно, U1 < U2. В этом случае, совершение внешней отрицательной работы на подачу газа к дросселю привело к увеличению U. Это повышение уровня U может с избытком компенсировать уменьшение ее кинетической части при обязательном возрастании потенциальной, что приведет к повышению температуры газа при дросселировании.
В точках инверсии (α i = 0) отрицательная работа проталкивания так увеличивает уровень внутренней энергии, что в точности компенсирует снижение кинетической части внутренней энергии из-за обязательного для дросселирования увеличения ее потенциальной части. Этим объясняется постоянство температуры в точках инверсии.
|
|
|
Таким образом, причиной возможного изменения температуры реального газа при дросселировании является возрастание потенциальной части его внутренней энергии, вызванное расширением газа.
|
|
|


