 |
1. Классификация по противомикробному спектру.
|
|
|
|
1. Классификация по противомикробному спектру.
ü Антибиотики широкого спектра (подавляют грамположительные кокки и грамотрицательные бактерии кишечной группы):
o полусинтетические аминопенициллины,
o карбоксипенициллины и уреидопенициллины,
o цефалоспорины III-V генераций, карбапенемы, циклосерин, рифампицин, аминогликозиды, тетрациклины, глицилциклины, хлорамфеникол.
ü Антибиотики условно широкого спектра (подавляют грамположительные кокки и внутриклеточные микроорганизмы): макролиды.
ü Антибиотики узкого спектра:
o подавляют грамположительные микроорганизмы: природные пенициллины, оксациллин, цефалоспорины I-II генераций, гликопептиды, липогликопептиды, бацитрацин, липопептиды, грамицидин С, линко замиды, мупироцин;
o подавляют грамотрицательные микроорганизмы: полимиксин В, противогрибковые полиеновые антибиотики, гризеофульвин.
2. Классификация по характеру противомикробного действия.
ü Бактерицидные ( вызывают гибель микроорганизмов): пенициллины, цефалоспорины, карбапенемы, гликопептиды, липогликопептиды, баци-трацин, липопептиды, полимиксин В, рифампицин, аминогликозиды.
ü Бактериостатические (останавливают размножение микроорганизмов): те-трациклины, глицилциклины, хлорамфеникол, линкозамиды, мупироцин.
ü Бактериостатические или бактерицидные в зависимости от дозы и вида микроорганизма: макролиды, циклосерин.
ü Фунгицидные и фунгистатические: противогрибковые полиеновые антибиотики, гризеофульвин.
3. Классификация по механизму противомикробного действия.
ü Антибиотики, нарушающие синтез клеточной стенки микроорганизмов: пенициллины, цефалоспорины, карбапенемы, гликопептиды, липогли-копептиды, циклосерин, бацитрацин.
|
|
|
ü Антибиотики-детергенты, нарушающие проницаемость цитоплазмати-ческой мембраны микроорганизмов: полимиксин В, грамицидин С, ли-попептиды, противогрибковые полиеновые антибиотики.
ü Антибиотики, нарушающие транскрипцию матричной РНК: рифампицин.
ü Антибиотики, нарушающие синтез белка (трансляцию) на рибосомах:
o на 30S-субъединице: аминогликозиды, тетрациклины, глицилциклины;
o на 50S-субъединице: макролиды, хлорамфеникол, линкозамиды.
ü Антибиотики, нарушающие митоз у грибов: гризеофульвин.
По клиническому применению выделяют
ü основные
ü резервные антибиотики.
Основные антибиотики оказывают
ü наиболее выраженное противомикробное действие на патогенные микроорганизмы
ü лучше переносятся больными.
Резервные антибиотики назначают
ü при резистентности микроорганизмов к основным антибиотикам или их опасном побочном действии.
При внебольничных инфекциях часто проводят эмпирическую антибио-тикотерапию без бактериологического исследования и определения чувствительности микроорганизмов к антибиотику. Этиологию заболеваний и чувствительность возбудителей можно предвидеть в зависимости от региональных особенностей. Возбудители госпитальных (внутрибольничных, нозокомиаль-ных1) инфекций обладают высокой резистентностью к обычно применяемым антибиотикам, для адекватного выбора антибиотика необходим бактериологический анализ.
антибиотики, нарушающие синтез клеточной стенки микроорганизмов (бактерицидные)
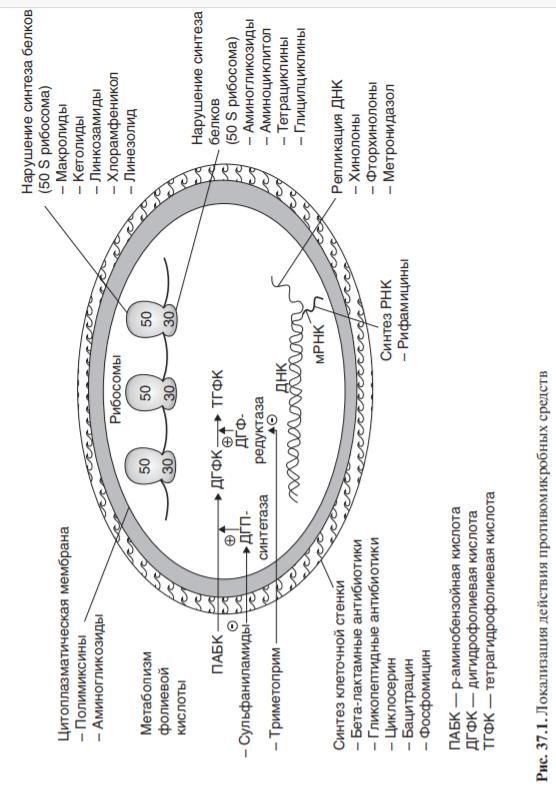
АБ Нарушают синтез клеточной стенки
β -Лактамные антибиотики
Антибиотики группы β -лактамов - пенициллины, цефалоспорины и карбапенемы - составляют около половины применяемых в мире антибиотиков.
ü Они нарушают синтез клеточной стенки микроорганизмов, их селективное действие обусловлено отсутствием такой стенки в клетках человека.
|
|
|
ü Антибиотики группы β -лактамов оказывают бактерицидное действие преимущественно на размножающиеся микроорганизмы, поэтому нерационально их совместное применение с бактериостатическими средствами, останавливающими размножение.
Антибиотики группы пенициллина
Пенициллины представляют собой полярные гидрофильные дипептиды, производные 6-аминопенициллановой кислоты, состоят из тиазолидинового и β -лактамного колец.
Механизм бактерицидного действия пенициллинов
ü нарушение синтеза клеточной стенки микроорганизмов.
Строение клеточной стенки
ü У Г+ микроорганизмов клеточная стенка построена из 50-100 слоев пептидогликана - полимерного соединения N-ацетилмурамовой кислоты и N-ацетилглюкозамина.
ü Клеточная стенка Г- состоит из 1-2 слоев пептидогликана, снаружи от нее расположена мембрана, содержащая липополисахариды.
ü В цитоплазме микроорганизмов синтезируется УДФ-ацетилмурамил-пентапептид. Он присоединяет дипептид D-аланин-D-аланин и связывает УДФ-ацетилглюкозамин с освобождением уридиновых нуклеотидов. Образуются полимеры пептидогликана.
ü На цитоплазматической мембране микроорганизмов находятся пенициллинсвязывающие белки с активностью транспептидазы. У золотистого стафилококка известно четыре варианта пенициллинсвязывающих белка, у кишечной палочки - семь.
ü Поперечные связи пептидогликана сформированы мостиками из пяти молекул глицина.
ü Пентаглициновый мостик соединяет L-лизин N-ацетилмурамил-пентапептида с D-аланином в четвертом положении соседнего пептида. Для образования связи удаляется D-аланин, находящийся в пятом положении.
ü Разрыв связи между двумя молекулами D-аланина катализирует транспептидаза пенициллинсвязывающих белков. Активный центр фермента связывает дипептид D-аланин-D-аланин.



Пенициллины функции:
ü Пенициллины проникают к цитоплазматической мембране микроорганизмов и с помощью β -лактамного кольца взаимодействуют с пенициллинсвязывающими белками.
ü В процессе ковалентного связывания кольцо β -лактама раскрывается.
|
|
|
ü Стереоконфигурация пенициллинов близка к стереоструктуре дипептида D-аланин-D-аланин.
ü Антибиотики необратимо по конкурентному механизму ингибируют транспептидазную активность пенициллинсвязывающих белков.
ü Между линейными полимерами пептидогликана не формируются поперечные связи.
ü Появляются лишенные клеточной стенки протопласты. Они быстро подвергаются лизису под влиянием собственных протеолитических ферментов - аутолизинов и гидролаз.
ü Аутолизу способствует исчезновение из клеточной стенки липотейхоевых кислот - естественных ингибиторов гидролаз.
При необоснованно коротком курсе антибиотикотерапии появляются сфе-ропласты с частично построенной клеточной стенкой. Они могут достроить клеточную стенку и вызывать рецидив инфекции.
ü Бактерицидное действие пенициллинов направлено на расположенные вне клеток размножающиеся микроорганизмы.
ü Природные пенициллины преимущественно подавляют грамположительные микроорганизмы. Антибиотики хуже проникают через наружную мембрану грамотрицательных микроорганизмов из-за высокого содержания в ней липополисахаридов, а также быстро инактивируются β -лактамазами в периплазматическом пространстве вблизи пенициллинсвязывающих белков.
К антибиотикам группы пенициллина микроорганизмы приобретают резистентность. Ее механизмы:
ü уменьшение проницаемости пориновых каналов наружной мембраны;
ü появление высокомолекулярных пенициллинсвязывающих белков со сниженным аффинитетом;
ü гидролиз β -лактамазами;
ü ускоренное удаление (эффлюкс) из клеток;
ü низкая активность аутолитических ферментов и гидролаз;
ü замедленное деление микробных клеток.
β -Лактамазы вызывают гидролиз β -лактамного кольца пенициллинов. Информация об этих ферментах кодирована в плазмидах и хромосомах. β -Лактамазы узкого спектра - пенициллиназы и цефалоспориназы - инак-тивируют соответственно пенициллины и цефалоспорины, β -лактамазы широкого спектра разрушают обе группы антибиотиков, β -лактамазы расширенного спектра инактивируют также карбапенемы.
|
|
|
Антибиотики группы пенициллина классифицируют на природные (биосинтетические) и полусинтетические.
Природные (биосинтетические) пенициллины .


Препараты природного пенициллина оказывают бактерицидное действие преимущественно на Г+ бактерии:
· гемолитические стрептококки,
· пневмококк,
· коринебактерию дифтерии,
· бациллу сибирской язвы,
· клостридии,
· листерию,
· актиномицеты.
· менингококка, гонококка,
· трепонемы сифилиса,
· лептоспир
· боррелий.
Около 90% штаммов золотистого стафилококка продуцируют β -лактамазу, широко распространены резистентные штаммы пневмококка и гонококка. Активность природных пенициллинов выражают в единицах действия.
С Аляутдина:
β -Лактамные антибиотики (пенициллины, цефалоспорины, карбапенемы и монобактамы) — это ЛС, имеющие в составе молекулы β -лактамное кольцо (рис. 37. 2), которое необходимо для реализации противомикробной активности этих соединений. При расщеплении β -лактамного кольца

бактериальными ферментами (β -лактамазами) антибиотики утрачивают антибактериальную способность. Сходство химической структуры β -лактамов обусловливает одинаковый механизм действия.
β -Лактамные антибиотики — структурные аналоги группы D-Ала-D-Ала.
ü Антибиотики этой группы связываются с активным центром фермента и угнетают транспептидазы бактерий, вследствие этого нарушают синтез пептидогликана клеточной стенки бактерий. Кроме того, β -лактамы угнетают эндогенный ингибитор аутолизинов, активность аутолизинов повышается.
ü Аутолизины необходимы для расщепления пептидогликана при делении клетки. Ингибирование транспептидазы и активация аутолизинов приводят к аутоцитолизу и гибели клетки.
ü Поэтому, как правило, β -лактамы обладают бактерицидным действием в отношении активно делящихся бактерий. Растущие бактерии активно синтезируют пептидогликан и являются мишенью для действия β -лактамных антибиотиков.
ü В основе строения пенициллинов лежит 6-аминопенициллановая кислота. Пенициллины отличаются друг от друга строением радикала боковой цепи, присоединенного к остатку аминогруппы 6-аминопенициллановой кислоты.
ü Выделяют природные (биосинтетические) и полусинтетические пенициллины. Природные пенициллины Природные (биосинтетические) пенициллины образуются различными видами плесневых грибов рода Penicillium. Бензилпенициллин (рис. 37. 3) связывается с транспептидазой (ПСБ) бактерий.
|
|
|

Механизм антибактериального действия пенициллинов связан с:
ü блокадой фермента транспептидазы, обеспечивающей соединение цепей пептидогликана при помощи пентаглициновых мостиков, завершающей стадии синтеза пептидогликанового полимера;
ü угнетением эндогенного ингибитора аутолизинов, играющих ключевую роль в расщеплении пептидогликана при делении бактериальных клеток.
|
|
|


