 |
4.2.2 Закон Бугера-Ламберта-Бера
|
|
|
|
4. 2. 2 Закон Бугера-Ламберта-Бера
В основе количественного молекулярного анализа с использованием молекулярной спектроскопии лежит закон Бугера-Ламберта-Бера, связывающий интенсивность света падающего 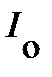 и прошедшего
и прошедшего  с концентрацией
с концентрацией  и толщиной поглощающего слоя
и толщиной поглощающего слоя  (рисунок 4. 2):
(рисунок 4. 2):
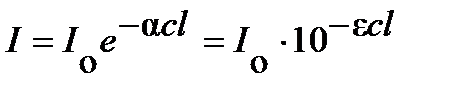 , ,
| (4. 16) |
где  и
и  - коэффициенты поглощения. Коэффициент
- коэффициенты поглощения. Коэффициент  часто называют коэффициентом экстинкции.
часто называют коэффициентом экстинкции.
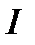
|

|

|
Рисунок 4. 2 – Иллюстрация закона Бугера-Ламберта-Бера
Закон Бугера-Ламберта-Бера может быть легко обоснован: уменьшение интенсивности света при прохождении через вещество  пропорционально
пропорционально  и числу частиц, встретившихся на пути пучка, т. е.
и числу частиц, встретившихся на пути пучка, т. е.  и
и  :
:
 ~ ~  . .
|
или с коэффициентом пропорциональности:

| (4. 17) |
Проинтегрируем полученное уравнение:
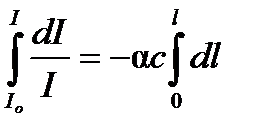
| (4. 18) |
Результат интегрирования:

| (4. 19) |
или
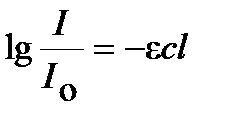 . .
| (4. 20) |
При уменьшении интенсивности падающего света на порядок
 . .
| (4. 21) |
Если  = 1 моль/л, то
= 1 моль/л, то 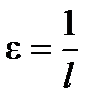 , т. е. коэффициент поглощения
, т. е. коэффициент поглощения 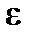 равен обратной толщине слоя, в котором при концентрации, равной 1, интенсивность падающего света уменьшается на порядок.
равен обратной толщине слоя, в котором при концентрации, равной 1, интенсивность падающего света уменьшается на порядок.
Коэффициенты поглощения  и
и  зависят от длины волны. Вид этой зависимости является своеобразным «отпечатком пальцев» молекул, что используется в качественном анализе для идентификации вещества. Эта зависимость характерна и индивидуальна для того или иного вещества и отражает характеристические группы и связи, входящие в молекулу.
зависят от длины волны. Вид этой зависимости является своеобразным «отпечатком пальцев» молекул, что используется в качественном анализе для идентификации вещества. Эта зависимость характерна и индивидуальна для того или иного вещества и отражает характеристические группы и связи, входящие в молекулу.
Оптическая плотность D
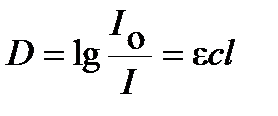
| (4. 22) |
обычно измеряется в максимуме поглощения, в соответствии с уравнением (4. 22) пропорциональна концентрации вещества, что используется в количественном анализе. После калибровки по системам (растворам) с известными концентрациями и построения калибровочного графика по измеренному значению  неизвестного раствора можно определить концентрацию
неизвестного раствора можно определить концентрацию  (рисунок 4. 3).
(рисунок 4. 3).
|
|
|
| D |
| Сх |
Рисунок 4. 3 – Определение концентрации раствора по оптической плотности
Закон Бугера-Ламберта-Бера выполняется не всегда. Причина – химические и межмолекулярные взаимодействия в растворах, а также инструментальные искажения.
Помимо оптической плотности, часто используют количественные величины: пропускание

| (4. 23) |
выражаемое в %
 , ,
| (4. 24) |
или поглощение 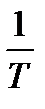 :
:
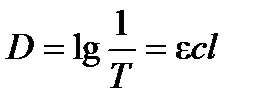
| (4. 25) |
4. 2. 3 Энергия вращения двухатомной молекулы в приближении жесткого ротатора. Вращательные спектры молекул и их применение для определения молекулярных характеристик
Появление вращательных спектров связано с тем, что вращательная энергия молекулы квантуется, т. е.
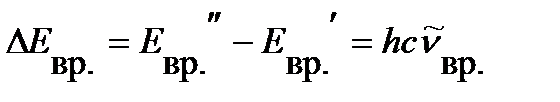 , ,
| (4. 26) |
где 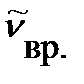 - волновое число линии во вращательном спектре.
- волновое число линии во вращательном спектре.
Рассмотрим механизм возникновения вращательного спектра двухатомной молекулы, межъядерное расстояние в которой постоянно. Такая система называется жестким ротатором.
| m1 |

|
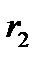
|

|

|

|

|
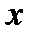
|
| 0 |
| а |

|

|

|

|
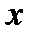
|
| 0 |
| б |
Рисунок 4. 4 – Модель жесткого ротатора
на примере двухатомной молекулы (а) и частицы (б)

|
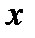
 , ,
| (4. 27) |
где  - угловая скорость вращения;
- угловая скорость вращения;  - момент инерции системы:
- момент инерции системы:
 . .
| (4. 28) |
Поскольку точка O является центром тяжести молекулы, то:
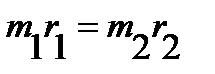 . .
| (4. 29) |
Учитывая, что
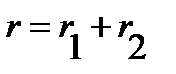
| (4. 30) |
равенство (4. 29) можно переписать относительно  или
или  :
:
 , ,  , ,
| (4. 31) |
|
|
|
 , , 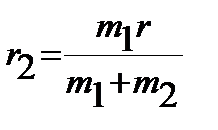 . .
| (4. 32) |
Подстановка полученных выражений в уравнение (4. 28) позволяет момент инерции I с межъядерным расстоянием  :
:
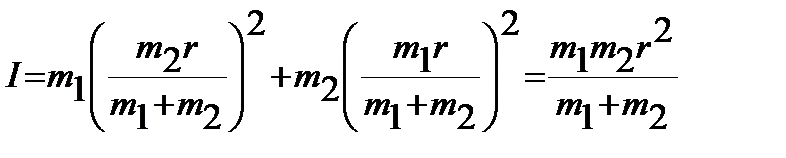 . .
| (4. 33) |
Введение обозначения приведенной массы  :
:

| (4. 34) |
приводит к уравнению
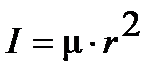 . .
| (4. 35) |
Таким образом, двухатомную молекулу (рисунок 4. 7а), вращающуюся вокруг оси 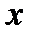 или
или  , проходящей через центр тяжести, можно упрощенно рассматривать как частицу с массой
, проходящей через центр тяжести, можно упрощенно рассматривать как частицу с массой  , описывающую круг с радиусом
, описывающую круг с радиусом  вокруг точки O (рисунок 4. 7б).
вокруг точки O (рисунок 4. 7б).
Вращение молекулы вокруг оси  дает момент инерции, практически равный нулю, поскольку радиусы атомов значительно меньше межъядерного расстояния. Вращение относительно осей
дает момент инерции, практически равный нулю, поскольку радиусы атомов значительно меньше межъядерного расстояния. Вращение относительно осей 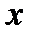 или
или  , взаимно перпендикулярных линии связи молекулы, приводит к равным по величине моментам инерции:
, взаимно перпендикулярных линии связи молекулы, приводит к равным по величине моментам инерции:

| (4. 36) |
Решение уравнения Шредингера для вращательной энергии в приближении модели жесткого ротатора дает уравнение:

| (4. 37) |
где  - вращательное квантовое число, принимающее только целочисленные значения
- вращательное квантовое число, принимающее только целочисленные значения
 = 0, 1, 2…. В соответствии с правилом отбора для вращательного спектра двухатомной молекулы изменение вращательного квантового числа при поглощении кванта энергии возможно лишь на единицу, т. е.
= 0, 1, 2…. В соответствии с правилом отбора для вращательного спектра двухатомной молекулы изменение вращательного квантового числа при поглощении кванта энергии возможно лишь на единицу, т. е.
 . .
| (4. 38) |
Введение вращательной постоянной  :
:

| (4. 39) |
преобразует уравнение (4. 37) в вид:
 . .
| (4. 40) |
Разность энергий двух соседних уровней может быть оценена по уравнению:

| (4. 41) |
Из анализа уравнения (4. 41) следует, что с ростом  возрастает
возрастает  , т. е. вращательные уровни расходятся. Напротив, увеличение
, т. е. вращательные уровни расходятся. Напротив, увеличение  приводит к уменьшению
приводит к уменьшению  .
.

|

|
 20
20  12
12  6
6  2
2 
|
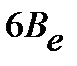
|

|

|
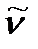
|

|
| а б |
Рисунок 4. 5 – Расположение вращательных уровней энергии (а)
и схематичный вид вращательного спектра двухатомной молекулы (б)
в приближении жесткого ротатора
Поскольку
 , ,
| (4. 42) |
волновое число линии во вращательном спектре, соответствующей поглощению кванта при переходе с j уровня энергии на уровень j+1, можно вычислить по уравнению:
 . .
| (4. 43) |
Из этого уравнения следует, что с ростом  волновое число линии во вращательном спектре
волновое число линии во вращательном спектре 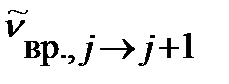 увеличивается, а интервал между линиями, тем не менее, остается постоянным:
увеличивается, а интервал между линиями, тем не менее, остается постоянным:
|
|
|

| (4. 44) |
Таким образом, вращательный спектр в приближении модели жесткого ротатора представляет собой систему линий, находящихся на одном и том же расстоянии друг от друга (рисунок 4. 5б). Примеры вращательных спектров двухатомных молекул, оцененных в модели жесткий ротатор, представлены на рисунке 4. 6.
| а б |


Рисунок 4. 6 – Вращательныe спектры HF (а) и CO(б)
Для молекул галогеноводородов этот спектр смещен в дальнюю ИК область спектра, для более тяжелых молекул – в микроволновую.
Исходя из полученных закономерностей возникновения вращательного спектра двухатомной молекулы, на практике сперва определяют расстояние между соседними линиями в спектре  , из которого далее находят
, из которого далее находят 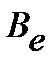 ,
, 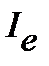 и
и 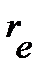 по уравнениям:
по уравнениям:
 , ,
| (4. 45) |
 , ,
| (4. 46) |

| (4. 47) |
Реальная молекула не является жестким ротатором, т. к. при достаточно высоких скоростях вращения связь в молекуле несколько растягивается в результате действия центробежных сил. При этом момент инерции увеличивается, а расстояние между линиями вращательного спектра двухатомной молекулы с ростом j уменьшаются.
Учет поправки на центробежное искажение приводит к некоторому усложнению уравнения для вращательной энергии:

| (4. 48) |
где 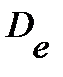 - постоянная центробежного искажения, связана с вращательной постоянной
- постоянная центробежного искажения, связана с вращательной постоянной 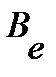 примерным соотношением
примерным соотношением  . Поправку следует учитывать лишь при очень больших j.
. Поправку следует учитывать лишь при очень больших j.
Для многоатомных молекул в общем случае возможно существование трех разных моментов инерции  . При наличии в молекуле элементов симметрии моменты инерции могут совпадать или даже быть равными нулю. Например, для линейных многоатомных молекул (CO2, OCS, HCN и др. )
. При наличии в молекуле элементов симметрии моменты инерции могут совпадать или даже быть равными нулю. Например, для линейных многоатомных молекул (CO2, OCS, HCN и др. )
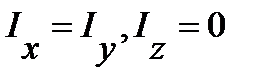
| (4. 49) |
В случае несимметричных линейных молекул существуют по крайней мере две различных длины связи, например, в молекуле OCS  . Для определения межъядерных расстояний в таких молекулах используют спектры изотопных заместителей. При изменении приведенной массы изменяется момент инерции и положение линий в спектре. Наблюдается изотопный сдвиг
. Для определения межъядерных расстояний в таких молекулах используют спектры изотопных заместителей. При изменении приведенной массы изменяется момент инерции и положение линий в спектре. Наблюдается изотопный сдвиг
|
|
|
 , ,
| (4. 50) |
где 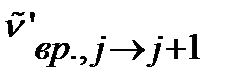 - положение линии, отвечающей вращательному переходу
- положение линии, отвечающей вращательному переходу  в изотопозамещенной молекуле.
в изотопозамещенной молекуле.
Для вычисления величины изотопного сдвига линии необходимо последовательно рассчитать приведенную массу 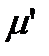 изотопозамещенной молекулы с учетом изменения атомной массы изотопа, момент инерции
изотопозамещенной молекулы с учетом изменения атомной массы изотопа, момент инерции 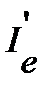 , вращательную постоянную
, вращательную постоянную  и положение линии в спектре молекулы по уравнениям (4. 34), (4. 35), (4. 39) и (4. 43), соответственно, или оценить отношение волновых чисел линий, отвечающих одному и тому же переходу в изотопозамещенной и неизотопозамещенной молекулах, и далее определить направление и величину изотопного сдвига по уравнению (4. 50). Если межъядерное расстояние приближенно считать постоянным
и положение линии в спектре молекулы по уравнениям (4. 34), (4. 35), (4. 39) и (4. 43), соответственно, или оценить отношение волновых чисел линий, отвечающих одному и тому же переходу в изотопозамещенной и неизотопозамещенной молекулах, и далее определить направление и величину изотопного сдвига по уравнению (4. 50). Если межъядерное расстояние приближенно считать постоянным  , то отношение волновых чисел соответствует обратному отношению приведенных масс:
, то отношение волновых чисел соответствует обратному отношению приведенных масс:

| (4. 51) |
Экстремальный характер зависимости интенсивности полос во вращательном спектре двухатомной молекулы (рис. 4. 6) может быть связан с относительной «заселенностью» вращательных уровней энергии. Реальный вращательный спектр является спектром не отдельно взятой молекулы, а большой совокупности частиц с различными и быстро меняющимися в результате соударений энергиями. Распределение молекул по энергиям при постоянстве внешних параметров постоянно и определяется распределением Больцмана.
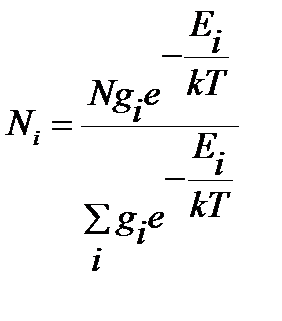 , ,
| (4. 52) |
где  - общее число частиц,
- общее число частиц, 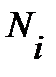 - число частиц на i - том уровне энергии при температуре T, k – постоянная Больцмана,
- число частиц на i - том уровне энергии при температуре T, k – постоянная Больцмана,  - статистический ве с или степень вырождения i-того уровня энергии, характеризует вероятность нахождения частиц на данном уровне.
- статистический ве с или степень вырождения i-того уровня энергии, характеризует вероятность нахождения частиц на данном уровне.
Для вращательного состояния заселенность уровня характеризуют обычно отношением числа частиц на j - том уровне энергии 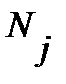 к числу частиц на нулевом уровне
к числу частиц на нулевом уровне  :
:
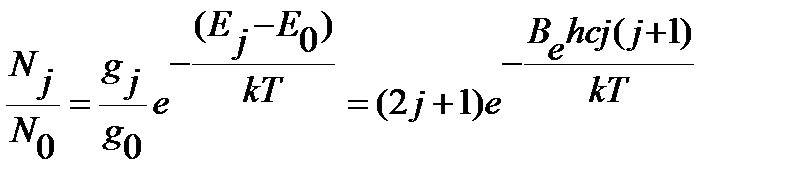 , ,
| (4. 53) |
где  - статистический вес j-того вращательного уровня энергии, отвечает числу проекций количества движения вращающейся молекулы на ее ось – линию связи молекулы,
- статистический вес j-того вращательного уровня энергии, отвечает числу проекций количества движения вращающейся молекулы на ее ось – линию связи молекулы,  , энергия нулевого вращательного уровня
, энергия нулевого вращательного уровня  . Функция
. Функция 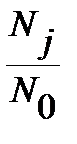 проходит через максимум при увеличении j, как иллюстрирует рисунок 4. 7 на примере молекулы CO.
проходит через максимум при увеличении j, как иллюстрирует рисунок 4. 7 на примере молекулы CO.
Экстремум функции соответствует уровню с максимальной относительной заселенностью, значение квантового числа которого можно вычислить по уравнению, полученному после определения производной функции в экстремуме:
 . .
| (4. 54) |
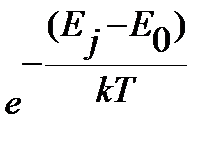


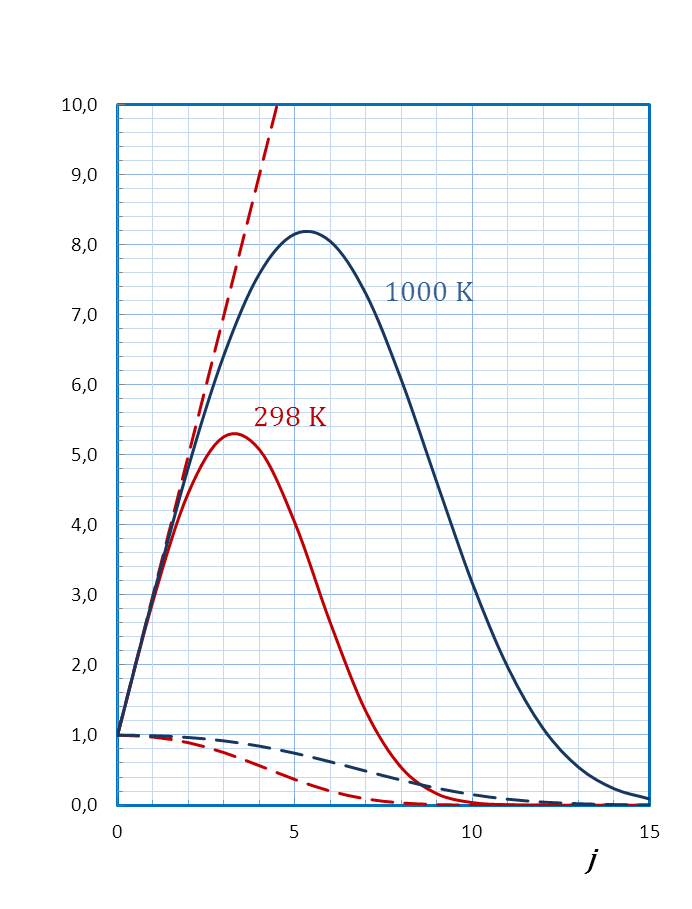
Рисунок 4. 7 – Относительная заселенность вращательных уровней энергии
молекулы CO при температурах 298 и 1000 К
|
|
|
Пример. Во вращательном спектре HI определено расстояние между соседними линиями  см-1. Рассчитайте вращательную постоянную, момент инерции и равновесное межъядерное расстояние в молекуле.
см-1. Рассчитайте вращательную постоянную, момент инерции и равновесное межъядерное расстояние в молекуле.
|
|
|


