 |
Распределение Максвелла. Распределение Больцмана
|
|
|
|
В состоянии термодинамического равновесия все направления скоростей молекул газа равновероятны вследствие хаотического теплового движения молекул. Модули скоростей молекул по той же причине различны из-за разнообразных столкновений молекул как между собой, так и со стенками сосуда и имеют вполне определенное статистическое распределение. Задача о распределении молекул газа по скоростям была поставлена и решена Д. Максвеллом (1859 г).
Пусть имеется газ, содержащий большое число молекул N. Внешние силовые поля, например сила тяжести, отсутствуют. Для решения поставленной задачи введем (рис. 9) пространство скоростей (импульсов). Скорость (импульс) каждой молекулы в какой-то момент времени t будем изображать точкой с координатами vx, vy, vz. Выберем в пространстве скоростей малый объем dw, содержащий достаточно большое количество точек (молекул).
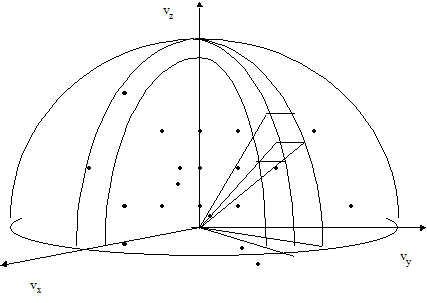
Рис. 9. Пространство скоростей и состояние молекул газа
Из-за теплового движения молекул точки будут двигаться в пространстве скоростей. Одни точки уходят из объема dw, другие, наоборот, приходят. В стационарном состоянии термодинамического равновесия число уходящих точек в среднем равно числу приходящих, и поэтому их число в малом объеме будет флуктуировать около некоторого среднего значения, которое мы обозначим dN. Это среднее значение dN, вероятно, будет различным в зависимости от того, где будет взят в пространстве скоростей малый объем dw. Выясним статистические закономерности, которым будет подчиняться dN. Величина, равная отношению числа точек (молекул) dN в малом объеме dw к общему числу точек (молекул) N, будет представлять вероятность dW нахождения точек в этом малом объеме.
|
|
|
dW = dN/N. (5.41)
Это есть вероятность того, что из всех N молекул газа dN молекул имеют скорости, проекции которых лежат в интервалах: от vx до vx + dvx, от vy до vy + dvy, от vz до vz + dvz. Величина, равная отношению вероятности dW нахождения точек в объеме dw пространства скоростей к этому объему, называется плотностью вероятности r(W) или функцией распределения молекул по скоростям f(v):
r(W) = f(v) = dN/(Ndw) = dW/dw. (5.42)
Замечание 1. Среднее число молекул, скорости которых имеют проекции, попадающие в указанные интервалы, равно dN = f(v)·N·dw. Если проинтегрировать это выражение по всему пространству скоростей (по возможным значениям), то получим полное число молекул газа N. 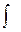 dN =
dN = 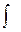 f(v)Ndw = N. Отсюда следует условие нормировки функции распределения:
f(v)Ndw = N. Отсюда следует условие нормировки функции распределения:
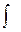 f(v)dw = 1. (5.43)
f(v)dw = 1. (5.43)
Совершенно очевидно, что вероятность того, что проекция скорости молекулы попадает в интервал от vx до vx + dvx пропорциональна dvx, а коэффициент пропорциональности зависит от vx: dWx = g(vx)dvx. Функция g(vx) называется функцией распределения молекул по проекциям скоростей. Аналогично:
dWy = g(vy)dvy и dWz = g(vz )dvz. Поскольку попадание молекулы в соответствующий интервал соответствующих проекций скоростей есть независимые события, то определенная ранее вероятность dW = dWx dWy dWz или f(v) = g(vx )g(vy)g(vz ), так как dvxdvydvz = dw. Ввиду изотропности газа, функция распределения f может зависеть только от квадрата модуля полной скорости, а функция g - от квадрата модуля соответствующей проекции скорости. Максвелл, взяв за основу гауссовское распределение случайных величин, показал, что функции распределения g и f имеют следующий вид:
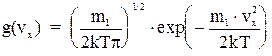 ,
,
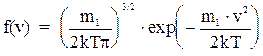 ,
,
где m1 - масса молекулы.
Эти функции называют функциями распределения Максвелла молекул газа соответственно по проекциям скоростей и по скоростям. Учитывая, что функция распределения молекул газа по скоростям не зависит от направления скоростей, можно получить распределение молекул газа по абсолютным значениям скоростей. Необходимо найти вероятность того, что модуль скорости лежит в интервале от v до v + dv. Эта вероятность равна dW = F(v)·dv. Точки, соответствующие таким молекулам в пространстве скоростей лежат внутри тонкого шарового слоя радиусом v и толщиной dv (рис. 9). Объем этого слоя равен dw = 4pv2dv. Поскольку плотность точек внутри этого слоя постоянна и равна f(v), то искомая вероятность будет равна dW = f(v)4pv2dv, а неизвестная функция F(v) = 4pv2f(v), или
|
|
|
 .
.
Функция F(v) должна удовлетворять условию нормировки:
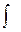 F(v)dv = 1.
F(v)dv = 1.
График функции F(v) имеет колоколообразный вид (рис. 10).

Рис. 10. Общий вид распределения молекул газа по скоростям
Используя функцию F(v), можно найти:
а) наиболее вероятную скорость молекул (vнв), при которой функция F(v) имеет максимальное значение:
vнв = 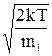 ,
,
б) среднюю арифметическую скорость молекул (vар):
vар = (1/N) 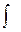 vdN =
vdN = 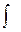 vF(v)dv =
vF(v)dv = 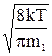 ,
,
в) среднюю квадратичную скорость молекул (vкв):
vкв = Ö1/N 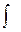 v2dN = Ö1/N
v2dN = Ö1/N 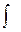 v2F(v)dv =
v2F(v)dv = 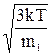 .
.
Замечание 2. Формулировка задачи о распределении молекул по скоростям и методы ее решения являются чисто классическими. Квантовые эффекты в газе начинают проявляться при низких температурах.
До сих пор мы рассматривали молекулы газа в отсутствии каких-либо силовых полей. В этом случае концентрация молекул газа в состоянии равновесия везде будет одинакова. Совсем иная картина будет, если молекулы находятся во внешнем силовом поле. Газ атмосферы находится в потенциальном поле силы тяжести. Если бы не было силы тяжести, то газ со временем весь рассеялся бы по Вселенной вследствие теплового движения. Если бы не было теплового движения, то все молекулы расположились бы на поверхности Земли. В конечном итоге тяготение и тепловое движение приводят к стационарному состоянию, при котором концентрация молекул и давление газа уменьшаются с возрастанием высоты над Землей.
Рассмотрим идеальный газ в однородном поле силы тяжести и находящийся в состоянии теплового равновесия при температуре T. Найдем закон изменения концентрации молекул газа с высотой над поверхностью Земли. Для этого рассмотрим условие равновесия бесконечно тонкого вертикального столба газа dh с площадью основания S, находящегося на высоте h (рис.11). В соответствии с законами механики сумма сил, действующих на выделенный объем должна быть равна нулю:
|
|
|
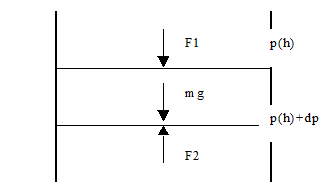
Рис. 11. Равновесие слоя газа в поле силы тяжести
-m1 gnSdh = [p(h) + dp]S - p(h)S. Откуда -dp = m1 gndh. Учитывая, что концентрация n = p/(kT), получим -dp = pm1gdh/(kT). Интегрируя и учитывая, что p(h = 0) = p0 получим барометрическую формулу:
p(h) = p0exp[-m1gh/(kT)].
Подставив основное уравнение молекуляряно-кинетической теории в барометрическую формулу, получим закон распределения числа молекул в единице объема (концентрации) по высоте:
n = n0exp[- m1gh/(kT)].
Если учесть, что в числителе показателя экспоненты стоит потенциальная энергия молекулы eP = m1gh, то получим закон распределения Больцмана (или просто распределение Больцмана):
n = n0exp[- eP/(kT)].
Замечание 3. Распределение Больцмана справедливо для всех потенциальных полей. Потенциальная энергия молекулы есть функция координат eP = eP(x,y,z). Концентрация молекул по определению n = dN/dV. Тогда dN/dV = n0exp[- eP/(kT)], где n0 - концентрация молекул в той области пространства, где потенциальная энергия eP = 0. Значение n0 пропорциональна общему числу молекул N. Учитывая это, можно записать: dN/N = a exp[- eP/(kT)] dV. Другими словами, получим вероятность того, что молекула находится в элементе объема dV, расположенном вблизи точки с координатами x,y,z.
dW(x,y,z) = a exp[- eP(x,y,z)/(kT)]dV.
Согласно распределению Максвелла, вероятность того, что скорости молекул находятся в элементе объема скоростного пространства dw, равна
dW(vx,vy,vz) = b exp[- eК(vx,vy,vz )/(kT)]dw.
Тогда вероятность того, что координаты молекулы попадают в интервалы: от x до x + dx, от y до y + dy, от z до z + dz, а проекции скоростей: от vx до vx + dvx, от vy до vy + dvy, от vz до vz + dvz , определится следующим образом:
dW = dW(x,y,z)dW (vx,vy,vz) = a b exp[- (eP + eК)/(kT)]dwdV.
Окончательно получим формулу, которая описывает распределение Максвелла-Больцмана классических частиц по состояниям с определенными значениями координат и проекций скоростей (импульсов):
dW = a b exp[-e/(kT)]dwdV,
где e = eP + eК - полная энергия частицы.
|
|
|


