 |
Ход работы. Контрольные вопросы. Работа № 9. Количественное определение крахмала. где С - содержание пектиновой кислоты (%);
|
|
|
|
Ход работы
25 г свежего материала (яблоки, сахарная свекла) растирают с битым стеклом или кварцевым песком в фарфоровой ступке до однородной массы, переносят в коническую колбу на 500 мл, заливают 100 мл воды, нагретой до 45°С (не выше), и выдерживают (при периодическом перемешивании и взбалтывании) 30 мин. при этой же температуре на водяной бане. Затем колбу плотно закрывают каучуковой, пробкой и энергично взбалтывают 15-20 мин.
После этого содержимое колбы отфильтровывают и собирают прозрачный раствор пектина. Для обеспечения полноты извлечения растворимого пектина осадок повторно заливают 75 мл воды и получают второй экстракт; в третий раз заливают 50-60 мл воды, каждый раз отделяя растворимый пектин от осадка. Экстракты объединяют, доводя их общий объем до 250 мл. Растворимый пектин определяют пектатным методом. Он основан на гидролизе пектиновых веществ и осаждении полигалактуроновой кислоты в виде пектата кальция.
В коническую колбу или химический стакан емкостью 500 мл отмеряют пипеткой 25 мл раствора пектина и приливают 100 мл 0, 1 Н раствора гидроксида натрия. Оставляют на 30 мин. для омыления растворимого пектина, который переходит в натриевую соль пектиновой кислоты. Затем добавляют 50 мл 1 Н раствора уксусной кислоты и получают свободную пектиновую (полигалактуроновую) кислоту. К полученной таким образом пектиновой кислоте через 5 мин, прибавляют 50 мл 2 Н р-ра СаС12 и оставляют стоять на 1 ч. За это время выпадает осадок пектата кальция. Осадок фильтруют, промывают горячей водой на взвешенном фильтре (фильтр предварительно многократно промывают водой и высушивают до постоянной массы в сушильном шкафу при 100°С) до тех пор, пока не станет отрицательной проба на хлорид-ионы с 1%-ным раствором нитрата серебра. Осадок вместе с фильтром помещают в бюкс и доводят до постоянной массы в сушильном шкафу при 100°С. По разнице между первоначальной массой фильтра и массой его с пектатом кальция находят содержание последнего в 25 мл раствора пектата. Содержание пектиновой кислоты вычисляют по формуле:
|
|
|
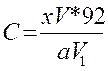
где С - содержание пектиновой кислоты (%);
х - количество найденного пектата кальция (г);
а - навеска исследуемого растительного материала (г);
V1- объем фильтрата, взятого для омыления и осаждения в
нем пектата кальция (мл);
V - начальный объем раствора пектина (мл);
92 - коэффициент пересчета (%), вычисленный исходя из
того, что пектат кальция содержит 8% кальция.
Контрольные вопросы
1. Что такое углеводы? Строение углеводов.
2. Перечислите основные функции углеводов.
3. На чем основана классификация углеводов?
4. Напишите уравнение химической реакции Троммера с глюкозой. Дают ли эту реакцию мальтоза и сахароза?
Работа № 9. Количественное определение крахмала
Реактивы: Оборудование:
картофель – 5 г, фарфоровая ступка с пестиком,
хлорид натрия, 10%-ный р-р, мерная колба (200 мл),
крахмал-индикатор 1%-ный р-р, стакан (150 мл),
соляная кислота, 25%-ный р-р, водяная баня под колбу,
р-р Люголя, стеклянная палочка,
0, 1 Н р-р йода, коническая колба (200 мл) с обратным серная кислота, 2 Н р-р, холодильником, стакан (250 мл),
сульфат натрия, 0, 1 Н р-р, воронка для фильтрования,
|
|
|
крахмал, 1%-ный р-р, пипетки (5 мл, 10 мл, 1 мл с меткой),
мерные цилиндры (25 и 100 мл),
термометр (400 С).
Химические методы определения крахмала основаны на измерении интенсивности его окраски с йодом, а также на определении количества образовавшейся глюкозы после его кислотного или ферментативного гидролиза. Метод, основанный на измерении интенсивности окраски крахмала с йодом, недостаточно точен в связи с тем, что взаимодействие это протекает различно у амилозы и амилопектина, а соотношение их в крахмале меняется в зависимости от объекта. Этот метод пригоден лишь для сравнительных определений. При использовании метода кислотного гидролиза необходимо количественное выделение крахмала из растительного материала ( при кислотном гидролизе расщепляются наряду с крахмалом целлюлоза, гемицеллюлозы и другие полисахариды, которых в растениях довольно много). Наиболее достоверные результаты получают при ферментативном расщеплении крахмала амилазой слюны. Количестве глюкозы, выделившейся при гидролизе крахмала, определяют йодометрически по Вильштеттеру и Шудлю.
Ход работы
5 г картофеля тщательно растирают в фарфоровой ступке, переносят в мерную колбу на 200 мл малым количеством холодной воды (30-50 мл) и туда же быстро вливают горячую дистиллированную воду (100 мл). Колбу сразу же помещают в кипящую водяную баню на 1 ч, чтобы полностью перевести крахмал в раствор. Содержимое колбы периодически перемешивают, при этом крахмальные зерна набухают и распадаются. Через 1 ч вынимают колбу из бани, охлаждают до 40°С и прибавляют 10 мл раствора слюны (см. работу № 4). Так как амилаза активируется хлорид-ионами, то в колбу добавляют 5 мл 10%-ного раствора хлорида натрия. Ферментативный гидролиз ведут при температуре 37-40°С в водяной бане в течение 2-3 ч. Степень гидролиза крахмала и момент его завершения устанавливают по реакции крахмала о йодом. Для этого стеклянной палочкой из колбы достают каплю жидкости с твердыми частицами, переносят пробу на стеклянную пластину и приливают несколько капель раствора Люголя. Если при действии йода на пробу синего окрашивания не отмечается, колбу доводят водой до метки, тщательно перемешивают содержимое и фильтруют через сухой фильтр в сухой стакан или колбу.
|
|
|
Образовавшиеся в результате действия амилазы декстрины и мальтозу гидролизуют 2, 5 %-ным раствором соляной кислоты. Для этого берут 100 мл фильтрата и переносят его в коническую колбу емкостью 200 мл. Добавляют туда же 12 мл 25%-ной соляной кислоты и выдерживают колбу на кипящей водяной бане о обратным холодильником в течение 3 ч. По окончании гидролиза колбу охлаждают, раствор из конической колбы переносят в мерную колбу на 200 мл, споласкивая ее несколько раз водой, и доводят раствор в мерной колбе до метки. «В нем определяют содержание глюкозы йодометрически: берут 10 мл раствора, добавляют 15 мл 0, 1 Н раствора йода и затем медленно вливают при энергичном помешивании 25 мл 0, 5 М раствора NаОН до исчезновения окраски йода; через 10-15 мин в колбу прибавляют 5 мл 2 Н раствора НС1 и выделившийся йод титруют 0, 1 Н раствором тиосульфата натрия. Когда раствор станет соломенно-желтым, добавляют 1 мл (20-25 капель) на каждые 50 мл жидкости 1%-ного раствора крахмала. Параллельно ставят контрольный опыт, в котором вместо гидролизата берут такой же объем дистиллированной воды. Содержание крахмала (С) в продукте (%) рассчитывают по формуле:
 , где
, где
V - количество 0, 1 Н раствора тиосульфата, израсходованного на
титрование в контроле (мл);
V1 - количество 0, 1 Н раствора тиосульфата, израсходованного на
титрование в опыте (мл);
0, 009 - коэффициент пересчета результатов титрования на
содержание глюкозы;
а - навеска исследуемого материала;
0, 9 - коэффициент пересчета глюкозы в крахмале;
V2 - объем вытяжки из растительного материала (в данном случае 400 мл);
V3 - объем гидролизата, взятого для йодометрического определения глюкозы (10 мл).
В клубнях картофеля содержание сахара незначительно (0, 1-0, 2%), поэтому им можно пренебречь и все найденное содержание глюкозы пересчитывать на крахмал. В другом материале (незрелые яблоки, листья, стебли) содержание сахара более значительно. Чтобы получить точные данные о содержании крахмала в этом случае, необходимо в отдельной навеске определить количество редуцирующих моно- и дисахаридов и полученную величину затем вычесть из результатов определения глюкозы, после чего провести пересчет ее на крахмал.
|
|
|


