 |
Липоиды с другими отрицательными полярными группами 3 Глава
|
|
|
|
| Количество элемента на должном уровне | Количество элемента на более высоком уровне | Объяснение: возникновение на должном уровне |
| высокий низкий высокий низкий | высокий высокий низкий низкий | количественный избыток качественная недостаточность избыточное качественное использование количественный дефицит |
С практической точки зрения, нам требуется информация, как о количестве элемента на должном уровне, так и на более высоком. Мы установили, что для элементов, относящихся к клеточному уровню, подобная информация может быть получена путем сравнения количеств в плазме и клетках красной крови (или цельной крови). При этом важно не соотношение между указанными величинами, как часто считают, а, скорее, сами величины. Для изменений на системном уровне допустимо сравнение между кровью и мочой, если учесть, что последняя соответствует сверхсистемному уровню.
Важность указанной концепции может быть продемонстрирована на следующих примерах. Калий представляет собой элемент клеточного уровня. При раке в условиях дисбаланса типа А, калий присутствует в ненормально большом количестве в пролиферирующих клетках. Он также обнаруживается в больших количествах в клетках красной крови. В указанных случаях калий обнаруживается в низких величинах на иерархически более высоком уровне в плазме крови или сыворотке. Нарушение заключается не только в простой гипокалиемии, а в избыточном использовании калия на клеточном уровне, низкое количество калия в клетках красной крови также укажет на дефицит калия. Высокое содержание калия в сыворотке и клетках красной крови может интерпретироваться, как уже отмечалось ранее, как соответствующее количественному избытку. Уменьшение количества калия в клетках красной крови, вместе с избытком в сыворотке, указывает нa качественный дефицит на определенном уровне.
|
|
|
Мы получим истинную картину ситуации, если будем считать "качественный" избыток или дефицит, определяемые по способности образовывать должные соединения. Если же он представляет собой элемент как таковой, который должен быть назначен для исправления количественного дефицита, для преодоления качественного недостатка использования, избыточного использования и количественного избытка, должны быть изменены другие факторы. (Рис. 127)
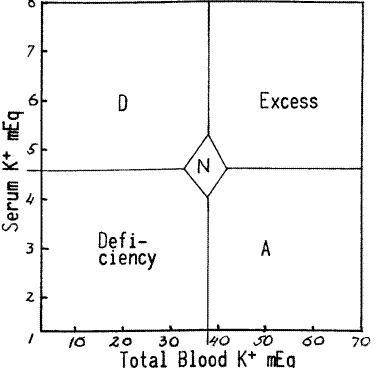
РИС. 127. Связь между количеством калия в сыворотке и цельной крови позволяет признать существующее состояние, находящимся в пределах нормы, количественном дефиците или избытке, или в дисбалансе типа А или D.
Хотя указанные связи представляют наиболее важный аспект фармакодинамики элементов, должны учитываться и другие. Избыток или дефицит элемента на высшем уровне, даже если он представляет биологическую защиту, борющуюся с нарушением на низшем уровне, сам по себе представляет проблему для высшего уровня. Тот факт, согласно которому элемент не принадлежит указанному уровню, придает его влиянию вредный характер. Влияние, оказываемое на чувствительные органы, часто вызывает важные патологические изменения. Гиперкалиемия, даже вызванная ненормально низким использованием калия на клеточном уровне, может вести к серьезным проблемам в функционировании нервной системы и сердца.
Другим важным аспектом реактивности элемента является его влияние на уровни, располагающиеся ниже определенного ему. Элемент, действующий на более низком уровне, обычно оказывает биологически противоположное действие тому, которое было свойственно на определенном ему уровне и поэтому оказывается отрицательным. На низшем уровне типы активности элемента А или D становятся противоположными себе.
|
|
|
Натрий, например, являющийся агентом типа А межклеточного компартмента, дает дисбаланс типа D на клеточном уровне, который иерархически расположен ниже по отношению к его собственному. Идентично, Mg, являющийся D-aгентом на своем собственном межклеточном уровне, обладает A-индуцирующей активностью на клеточном уровне.
Анализ фармакологии элементов в аспекте их A или D-индуцирующей активности, уровня, которому они принадлежат и соединений, через которые они действуют, еще находится на ранней стадии изучения, хотя и представляет многообещающую программу. В следующей таблице мы попытались интерпретировать данные, касающиеся элементов в аспекте А или D-индуцируемой активности. Мы начали с элементов Hm, обладающих D-индуцирующей активностью. Они повторяют в своем действии липоиды с отрицательной полярной группой. tаблица XVII представляет список элементов Hm или ряд D и связывает их через их периоды с организационными компартментами.
| таблица XVII hm элементы | ||||||||||
| Компартменты | Металлы | Неметаллы | ||||||||
| Органный | Be | С | О | |||||||
| Межклеточный | Mg | Si | S | |||||||
| Клеточный | Ca | Sc | V | Mn | Co | Cu | Ge | Se | Se | |
| Ядерный | Sr | Y | Nb | Tc | Rh | Ag | Sn | Те | Te | |
| Субморфологический | Ba | Та | Re | Ir | Au | Pb | ||||
| Первично биологический | Ce | Nd | Sm | Gd | Dy | Er | Yb | |||
| Субмолекулярный | Ra | Th | U | Pu | Cm | Cf | ||||
Мы уже обсуждали фармакологическую активность серы и селена через соединения, в которые они входят, и не будем здесь вновь это делать. Перед тем как приступить к анализу других элементов, следует вспомнить об основном характере их активности. Поскольку большая часть элементов действует через специфические соединения, факторы, определяющие вхождение элементов в специфические биологические комбинации, будут представлять первостепенное значение. Доступность элемента самого по себе является всего лишь одним фактором в его фармакодинамике. Учитывая выше изложенное, мы исследовали некоторые элементы из указанной группы Hm.
Мы мало знаем о каких-либо воздействиях на организм, как объект, бериллия в качестве металла. Его токсические эффекты являются следствием активности ненормальных количеств на низших уровнях. В этом же периоде таблица элементов есть два неметалла, углерод и кислород, для которых определенным для них уровнем является организм. Общая фармакологическая природа кислорода обусловлена ролью окисления в метаболических изменениях. Окисление представляет собой первую ступень в направлении катаболических, гомотропических изменений. Респираторная фаза в метаболизме углеводов, окислительное расщепление жирных кислот и окислительное дезаминирование аминокислот представляют примеры фундаментальной гомотропической интервенции кислорода.
|
|
|
Действуя на системном уровне, непосредственно ниже собственного, кислород оказывает иное действие. В соответствии с упоминавшемся выше правилом, кислород, являющийся на определенном ему уровне D aгентом, в крови будет обладать А активностью, которую мы будем изучать ниже вместе с другими А агентами. Гомотропическая связь кислорода с жирными кислотами обсуждалась выше при изучении биологической роли указанных веществ.
Связь между CO2 и жирными кислотами также представляет интерес. Большие количества свободных жирных кислот в крови обеспечивали лучшее присоединение CO2 к гемоглобину, также как большие количества стеринов действуют по отношению к кислороду. Мы исследовали указанную связь между CO2 и жирными кислотами, удерживая жирную кислоту, такую как линоленовую, в атмосфере CO2 соединенной с манометром. Результатом было очень заметное отрицательное давление. Венозная кровь, богатая CO2, в которой также превалируют жирные кислоты, теряет CO2 и жирные кислоты при прохождении через легкие.
Магний
Среди элементовII A ряда периодической таблицы, вызывающих дисбаланс D, первым мы изучили магний, относящийся к межклеточному компартменту и, таким образом, связанному с морем, как исходной средой. Большая часть активности указанного элемента может интерпретироваться как D индуцирующая. Mg во многих отношениях является антагонистом по отношению к Na, катиону того же компартмента, члену ряда, которому свойственен характер, противоположный А индуцирующему. Высокое содержание Mg, обнаруживаемое в крови, было связано с надпочечниковой недостаточностью, (127) в то время как низкие уровни Mg обычно наблюдают при высоком содержании в крови холестерина. (128)
|
|
|
Установлено, что избыток Mg вызывает адреналовый дефицит. Мы объясняли указанное действие существующим антагонизмом между Mg и Na. Таким образом, мы могли нейтрализовать благотворное действие NaCI у адреналэктомированных крыс путем парентерального назначения сульфата магния. Идентичный эффект был получен даже при пероральном применении тиосульфата магния. (Заметка 9)
Связь магния с защитным механизмом представляет особый интерес. Mg, возможно, вмешивается в литическое действие серы на клетки раковых асцитов (широко изучавшихся в нашей лаборатории R. Willheim, P. Fluss и M. Auber) (129) которое, как мы наблюдали, представляет характерный признак D индуцирующей активности. Подобным же образом, магний предупреждает тромбоз, действуя как антитромботический агент. Он не только предупреждает появление фибрина, частично препятствуя разрушению тромбоцитов (130);но также, способствуя лизису уже образовавшихся тромбов. (131) Таким образом, получается, что он представляет ценный агент для лечения тромбоза (132) Его попутное действие против холестерина привело к его использованию в профилактике и лечении коронарного тромбоза.
Оказывается, магний является частью иного защитного механизма, неспецифического, представленного системой пропердина. Пропердин активен лишь в присутствии магния, ни Ca, ни Na не могут заменить его. (133) Более высокое содержание магния увеличивает активность пропердина.
Иногда наблюдается параллелизм между действием магния и Cu, другого D индуцирующего элемента. У животных, слишком долго вскармливаемых молоком, этот способ питания приводит к дисбалансу типа A, количество магния падает вместе с количеством Cu. Содержание магния в крови мало у людей с судорогами. (134) Mg оказался особенно эффективным в профилактике и лечении "травяной тетании" у животных, которая часто встречается при питании травой с высоким содержанием калия. (135)
Магний имеет идентичный антагонизм по отношению к К, и это может объяснить его противораковую активность. При раке наблюдают величины магния ниже нормальных, и наоборот, содержание калия высоко. Последний является А индуцирующим элементом, а низкое содержание магния, вероятно, способствует росту рака. Влага увеличивает количество К и снижает количество Mg в растениях, указанный факт связан с частотой рака, присущей разным географическим областям. (136) Различие между профилактическим и лечебным воздействиями магния особенно интересно. Назначенный после применения канцерогена, магний уменьшает процент индукции рака. (137, 138) Тем не менее, влияние его минимально в случаях уже возникшего или пересаженного рака, а также в случаях спонтанных опухолей.
|
|
|
Ниже мы обсудим вопрос возникновения рака вместе с действием других элементов.
Необходимо иметь в виду, при выборе неспецифических комбинаций, в которых предстоит назначать медикамент, что D индуцирующая активность магния особенно демонстративна на межклеточном уровне. Сульфат магния оказался пригодным для парентерального применения, в то время как тиосульфат - для перорального. В указанных формах, Mg, как мы наблюдали, индуцирует заметный локальный алкалоз в рН струпа раны второго дня и оказывает благотворные эффекты на боль кислотной модели. Заметное влияние на вызванные тиамином судороги у крыс и мышей побудило нас использовать тиосульфат магния в качестве инструмента лечения не только тетании, но и судорог. Он оказался эффективным в предотвращении эпилептических припадков и оказался полезным даже в случаях эпилептического статуса. Мы успешно применили один и тот же препарат при раке и претерминальных состояниях, соответствующих дисбалансу А. Менее важные эффекты наблюдались при использовании сульфата магния и тиосульфата магния на более низких уровнях.
Кальций
Биологическая активность кальция, другого члена ряда II A и D индуцирующего элемента, относящегося к клеточному уровню, также представляет интерес.
В своей абсорбции травой из почвы, Ca идентичен Mg, другому D индуцирующему элементу. Таким образом, травяная тетания индуцируется высоким К и низкими величинами Ca и Mg. Ca, являющийся другим D индуцирующим элементом, как и медь антагонистичны по отношению к цинку, A индуцирующему элементу. Мы наблюдали, что рак встречается реже в так называемых кальциевоглинистых областях, где почва формируется известняком. (139) Вместе с другими минералами, оптимальное содержание кальция в почве может помочь предупредить рак. В то время как SiO2 благоприятствует раку, Ca, как оказалось, предупреждает его. Кальций также является антагонистом цинка, который в высоких дозах, вероятно, благоприятствует развитию рака. (140) Связь между Ca и К позволила нам уточнить роль Ca в патогенезе рака, в противоположность K, который увеличивается в опухолях на почти 60% с уменьшением содержания кальция на 44%. (141-147)
Сопоставляя изменения K и Ca, интересно посмотреть, на счет какого из элементов можно непосредственно отнести увеличение злокачественных новообразований. При регенерации клеток печени, при которой происходит быстрый рост без развития злокачественного новообразования, калий увеличивается, в то время как кальций не меняется. Подобным же образом в других быстро растущих, но нормальных, клетках кальций не уменьшается, в то время как К увеличивается. Таким образом, калий оказывается связанным с процессом клеточного роста и размножением, который представляет также дополнительный фактор перехода от неинвазивного к инвазивному раку. Тем не менее, калий непосредственно не связан с раковым характером клеток. С другой стороны, уменьшенное количество кальция оказывается свойственно раковому процессу. (147) Уменьшенное содержание кальция при раке не является следствием недостатка элемента в организме, поскольку кальций не только доступен, но даже явно присутствует в избытке на системном уровне. Как мы установили, высокий кальциевый индекс мочи, указывающий на увеличенную экскрецию, присутствует при дисбалансе типа A. Нарушение состоит в низкой способности раковых клеток присоединять и правильно использовать кальций. Если кальций действует на поверхности клетки и его недостаток уменьшает клеточную адгезию, (148, 149) недостаток клеточного кальция увеличивает инвазивность раковых клеток и тенденцию к метастазированию. Дефицит кальция в клетках оказывается связанным со свойством молодости, в то время как избыток, вероятно, приводит к быстрому старению.
Таким образом, нарушение, вызванное качественным дефицитом кальция, происходит на клеточной поверхности. С ней связаны также проявления на тканевом уровне.
Назначение любой кальциевой соли вызывает явное увеличение местного алкалоза (Рис 128) рН струпа раны второго дня. Интересно, что в костных поражениях, особенно в метастазах костного рака, дисбаланс типа А характеризуется остеолитическим процессом, а тип D - остеопластическим. Местный ацидоз, присутствующий в поражениях с дисбалансом типа А объясняет мобилизацию кальция при указанных остеолитических процессах. Ca откладывается в значительных количествах в метастазах при дисбалансе типа D, что может быть связано с местным алкалозом, происходящим из нарушенного метаболизма. Указанный алкалоз представляет состояние, благоприятствующее выпадению кальция. Косвенно, отложение кальция в костных метастазах, как оказывается, соответствует модели D тканевого нарушения. Даже в этом случае для кальция характерна D индуцирующая активность.
При избыточной экскреции кальция с мочой проблема кальциевой фармакологии при раке типа А связана с формой, в которой он действует на клеточном уровне, где присутствует качественное нарушение. Поскольку количественное уменьшение должно рассматриваться как осложнение качественной недостаточности, а не общего количественного дефицита, проблема состоит не в даче кальция, а в поиске пути обеспечения лучшего использования на клеточном уровне. Именно поэтому назначение большинства солей кальция не оказывает влияния на развитие рака в клинике или эксперименте, но оказывает профилактическое действие на индукцию опухолей через канцерогены. Назначенный после инъекции канцерогена, кальций, как было показано, уменьшает процент положительных результатов. Назначенный после возникновения опухолей, кальций оказывает влияние минимальное или нулевое. Как мы показали ранее, чрезмерная экскреция кальция, сама по себе, достаточна, чтобы указать на дефицит использования кальция на клеточном уровне без дефицита кальция в организме. Показано лечение агентами, способными повлиять на присоединение кальция на клеточном уровне. Жирные кислоты, изменяющие клеточный метаболизм вплоть до индукции местного алкалоза, оказались наиболее активными агентами. Тестостерон и кальциферол оказались полезными, но не столь активными, как жирные кислоты.

Рис. 128. Влияние, оказываемое двумя элементами, калием и кальцием, на рН струпа раны второго дня, показывает явную тенденцию в направлении закисления для калия и ощелачивания для кальция. Для разных солей разница состоит в неравном влиянии, оказываемом анионом, усиливающим действие катиона.
В то время как высокая экскреция кальция с мочой указывает на дисбаланс типа А, низкая или отсутствующая экскреция с мочой может быть результатом чрезмерного использования клетками кальция или дисбаланса типа D на клеточном уровне. Могут использоваться другие анализы для выяснения указанного вопроса. При низкой экскреции кальция и указании других анализов на наличие дисбаланса типа D, все свидетельствует о том, что низкая экскреция является частью дисбаланса D. Если, наоборот, только экскреция кальция низка, а другие показатели соответствуют дисбалансу типа А, вероятно наличие количественного недостатка кальция в организме. Это можно корригировать назначением кальция парентерально или перорально в любой абсорбируемой форме. Низкая экскреция, также как и некоторые симптомы, могут быть преодолены за короткое время благодаря назначению достаточного количества кальция. В случае противоположного типа нарушения, с метаболической задержкой кальция, назначение кальция вызовет увеличение интенсивности симптомов.
Избыток кальция в моче, таким образом, соответствует низким значениям на клеточном уровне и необходимости присоединения кальция. Это вновь указывает на то, что проблема состоит не в количестве присутствующего кальция, а в дефиците его использования.
Медь
Медь из IB ряда - еще один анти-A элемент клеточного уровня, обязательный для синтеза из восстановленного гематина каталазы. Дефицит меди приводит к уменьшению активности этого энзима. Идентично, синтез гемоглобина возможен только в присутствии меди. Цитохромоксидаза содержит Fe и Cu. Дефицит Cu уменьшает печеночную цитохромоксидазу (150, 151, 152) Cu присутствует в сыворотке крови, связанной с белком с образованием церулоплазмина, который также действует как оксидаза. (153) Cu, благоприятствуя синтезу указанных веществ, вмешивается в конце концов в процессы, приводящие к активному катаболическому вмешательству кислорода. При этом, Cu действует как D индуцирующий агент. Cu активно вмешивается в метаболизм серы. (154, 155) Трансформация сульфгидрила в дисульфид замедлена и неполна при дефиците меди. Этот же дефицит уменьшает образование фосфолипидов, как это видно на печени крыс. (156) Косвенно, Cu благоприятствует анти-A активности.
Влияние Cu на обмен Ca также является косвенным. Мы наблюдали, что локальное отложение кальция в костях соответствует местной модели D. Недостаток меди, D индуцирующего агента, способствует появлению местных A состояний, которые, в случае кости, приведет к недостатку кальция, то есть к явлению, противоположному тому, что наблюдали при местном дисбалансе D. Указанная связь объясняет, почему, несмотря на достаточное количество P и Ca, недостаток меди индуцирует остеомаляцию с костным переломом и симптомами рахита, как это наблюдается у животных с косвенным дефицитом Cu, вызванного избытком молибдена (157, 158, 159), А индуцирующего агента. Назначение меди помогает вылечить указанные переломы. (157) Одновременное уменьшение Cu и Mg происходит у вскармливаемых молоком телят. (160) Обогащенность цинком, как и молибденом, может спровоцировать дефицит Cu и Ca. При дефиците меди и низкой каталазе сопротивляемость инфекциям снижается. При бруцеллезе дефицит Cu и Ca встречается вместе с уменьшенными концентрациями Mn и Co в крови и слюнных железах. (161, 162, 163) Сu, Са, Mn и Co - все являются металлами D индуцирующей группы.
При раке обнаруживается качественный дефицит меди. Как в раковых клетках, так и в печени больных раком, наблюдается явное уменьшение содержания каталазы. (164, 165) С другой стороны, содержание Сu значительно увеличивается в крови этих субъектов, причем отмечаются даже значения в три раза выше нормы. (166, 167, 168) Указанные показатели возвращаются к норме при исчезновении раковой опухоли. (169)
При раке дефицит меди на уровне клеток прослеживается явно, что видно не только по уменьшенной каталазе, но также по расстройствам в цитохром оксидазной системе, системе гематина, метаболитах SH и фосфолипидах. Дефицит этот, тем не менее, только локальный, а затем и качественный, поскольку избыток Сu обнаруживается непосредственно на более высоком уровне, в крови.
Локальное нарушение, заключающееся в неадекватной способности использовать медь, таким образом, связано с раком. У нормальных животных избыточная медь может быть использована и способна предупредит возникновение опухолей. Это объясняет, почему Сu, защищающая крыс от канцерогенных нитрокрасок, (170, 171, 172) не влияет на опухоли, если они уже были индуцированы, то есть, если имеется качественная недостаточность. Распознавание указанной разницы между формой, в которой медь используется нормальным животным, и дефицитом в раковых объектах, составило основу изучения этой ключевой проблемы патогенеза рака. Лечебное применение меди и других элементов, которое мы обсудим ниже, является не количественной, а качественной проблемой.
Марганец и кобальт
Два других элемента клеточного компартмента привлекли наше внимание. Марганец, благодаря вмешательству в качестве катализатора в процессы, приводящие к активации кислорода, косвенно демонстрирует D индуцирующий характер. Отмечено его присутствие в меньших количествах в опухолях или раковых органах, чем в контролях. Также как и с медью, не было отмечено эффектов в лечении опухолей соединениями марганца, хотя было получено некоторое превентивное действие в отношении опухолей, вызванных канцерогенами. Подобным же образом мы получили некоторое профилактическое действие, направленное против индукции опухолей канцерогенами, но не воздействие на развитие уже возникших опухолей. Не было установлено воздействия на пересаженные опухоли.
Более тяжелые элементы
Мы изучили активность элементов, соответствующих низшим уровням—таких как стронций и олово на ядерном; барий, золото и свинец - на субморфологическом; и цезий - на первичном биологическом компартментах. Чем ниже уровень элемента, тем больший профилактический эффект обнаруживался в отношении индукции опухолей канцерогенами. Тем не менее, как и прежде, был минимальным или отсутствовал эффект на клетки уже существующих опухолей.
Как уже нами отмечалось, мы соединили указанную парадоксальную активность с фактом, согласно которому нормальные клетки способны производить соединения, предупреждающие появление ракового объекта. Указанные соединения уже не формируются, если объект уже стал раковым.
Указанные положения образовали основу для целого ряда исследований роли разных элементов в патогенезе рака.
Элементы патогенеза рака
Были проведены исследования по сравнению количества и формы элемента, присутствующего у нормального животного и у пораженного раком. Наблюдались количественные и, особенно, качественные отличия, указывающие на место нарушения, большей частью ответственного за недостаток влияния, оказываемого элементом. Указанные результаты объясняют, почему назначение одного элемента недостаточно для оказания влияния на развитие уже появившегося ракового процесса. Еще более интересно, что они показывают, какое соединение элемента может оказать влияние. Указанное исследование, еще не законченное, открывает возможности их клинического применения. Именно через подобные соединения, присутствующие у нормальных, и недостающие у пораженных раком животных, были предприняты попытки повлиять на развитие рака. Важным этапом было обнаружение подходящих соединений, получаемых после обработки некоторыми элементами свежих органов in vitro. Их изучение может сделать возможным синтез подходящих компонентов. Ряд результатов, уже полученных в экспериментах на животных, подтверждает, что D-индуцирующая активность представляет фактор, встречающийся в перспективных в указанном плане элементах.
ГЛАВА 13 ФАРМАКОДИНАМИЧЕСКАЯ АКТИВНОСТЬ (ЧАСТЬ ВТОРАЯ)
ГРУППА АНТИЖИРНЫХ КИСЛОТ
Одновременно с исследованием агентов, способных корригировать дисбалансы типа A, внимание направляли на агенты, могущие повлиять на противоположный дисбаланс, типа D. Поскольку жирные кислоты вовлечены в патогенез дисбаланса типа D, в качестве корригирующих веществ должны изыскиваться те, которые имеют антижирокислотные свойства. Некоторые из указанных веществ являются естественными составляющими организм веществами, используемыми им для корректировки нормального и ненормального вмешательства жирных кислот. Они были последовательно выделены и изучены. Синтетические агенты также были получены и изучены, причем их выбор был обусловлен по большей части механизмом коррекции, использовавшемся организмом.
Составляющие антижирных кислот
Мы наблюдали, как свободные жирные кислоты теряют большую часть своей биологической активности, когда их полярная группа связана с другим радикалом. Это побудило нас исследовать вещества, которые в естественных условиях связаны с жирными кислотами. Далее было обнаружено, что каждая из основных групп жирных кислот связана в организме со специфическими компонентами. Ненасыщенные жирные кислоты, главным образом, связаны с глицерином, низшие ненасыщенные кислоты - с глицерофосфорными кислотами в качестве лецитинов, а высшие ненасыщенные кислоты - со стеринами. Конъюгированным жирным кислотам, обнаруживаемым при патологических состояниях, как оказалось, противостоят неоглюкогенные кортикоиды. Эти компоненты рассматривались в качестве естественно возникающих антижирокислотных веществ, и мы на первом этапе изучали, каким образом они участвуют, с целью установления равновесия активности жирных кислот, особенно, если последние действуют в качестве патогенетических факторов.
В указанном исследовании изучались два типа влияний: oдин, относительно прямой эффект, индуцированный через нейтрализацию энергетических центров, приводящий к более или менее завершенному процессу инактивации жирных кислот; второй, когда достигается косвенный эффект через изменения в процессах метаболизма, в который вмешиваются жирные кислоты. При особом виде вмешательства антижирная кислота, с которой связана жирная кислота, направляет ее биологические превращения к конечному пункту. Например, связь с глицерином благоприятствует метаболизму калорий. Связь с глицерофосфорным ионом конвертирует жирную кислоту, как насыщенную, так и ненасыщенную, в организационный компонент. Связь со стеринами благоприятствует функциональной роли, даже для моноэтеноидов.
Мы приступили к изучению естественно встречающихся антижирных кислот с тех агентов, которые, как известно, связаны в организме с жирными кислотами. Простейшим из указанных агентов является глицерин.
Глицерин
Глицерин представляет наиболее часто встречающееся в природе вещество, связанное с жирными кислотами. Мы пытались объяснить указанный факт, основываясь на структуре глицерина и его особой биологической роли. Нами было показано, что молекулы жирных кислот занимают взаимные параллельные положения при образовании ими мономолекулярных слоев. Благодаря их связи с глицерином, указанные молекулы жирных кислот консервируют указанную взаимную связь. (Рис. 129) Это может объяснить, почему в организме связь жирной кислоты и глицерина обеспечивает триглицерид, а моно и диглицериды представляют лишь промежуточные этапы.
|
|
|


