 |
1.1. Основные понятия и определения
|
|
|
|
1. 1. Основные понятия и определения
Термодинамическая система
Объектом изучения термодинамики является термодинамическая система. Под понятием системы подразумевается тело или совокупность тел. Система называется закрытой, если она сохраняет постоянное количество вещества при всех происходящих в ней изменениях; если нет, то систему принято называть открытой.
Если между системой и окружающей ее средой нет каких-либо энергетических взаимодействий, то такую систему принято называть изолированной системой.
Система, состоящая из одной фазы вещества или веществ, называется гомогенной. Гомогенная система, неподверженная действию гравитационных, электромагнитных и других сил и имеющая во всех своих частях одинаковые свойства, называется однородной.
Система, состоящая из нескольких гомогенных частей (фаз), отделенных поверхностью раздела, называется гетерогенной.
Термодинамической системой принято называть закрытую систему, внутреннее состояние которой определяется N = n +1 независимыми переменными (n-деформационные координаты и T – абсолютная температура), связь между параметрами называется уравнением состояния, в случае простого тела (реальный газ) состояние системы характеризуется двумя попарно независимыми параметрами в этом случае уравнение состояния в неявном виде имеет следующий вид F(р, v, T) = 0. Состояние идеальной системы (идеальный газ) вполне определяется одним параметром-абсолютной температурой.
Если состояние термодинамической системы и ее параметры не изменяются во времени, то говорят, что система находится в равновесном состоянии.
Равновесным состоянием системы называется такое состояние системы, которое может существовать сколь угодно долго при отсутствии внешнего воздействия.
|
|
|
Параметры состояния
Параметры состояния - физические величины, характеризующие внутреннее состояние термодинамической системы. Параметры состояния термодинамической системы подразделяются на два класса: интенсивные и экстенсивные. Интенсивные свойства не зависят от массы системы, а экстенсивные - пропорциональны массе.
Термодинамическими параметрами состояния называются интенсивные параметры, характеризующие состояние системы.
К простейшим термодинамическим параметрам состояния относятся: удельный объем (  ), давление (
), давление ( 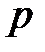 ) и температура (
) и температура ( 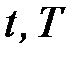 ).
).
Удельный объем( 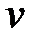 ) - это объем единицы массы вещества, а величина, обратная удельному объему, называется плотностью вещества (
) - это объем единицы массы вещества, а величина, обратная удельному объему, называется плотностью вещества ( 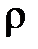 )
)
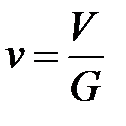 ; r
; r 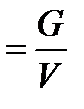 ;
; 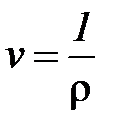 , (1. 1)
, (1. 1)
где V – объем, м3; G – масса вещества, кг; 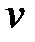 – удельный объем,
– удельный объем,  ;
;
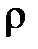 – плотность,
– плотность, 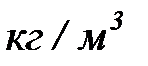 .
.
Отношение массы вещества (G) к его молярной массе ( 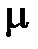 ) определяет число киломолей (кмоль) вещества
) определяет число киломолей (кмоль) вещества
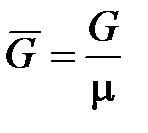 . (1. 2)
. (1. 2)
Объем киломоля вещества или молярный объем 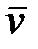 связан с удельным объемом следующим соотношением:
связан с удельным объемом следующим соотношением:
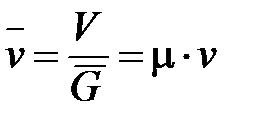 . (1. 3)
. (1. 3)
Абсолютное давление ( 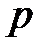 ) есть предел отношения нормальной составляющей силы к площади, на которую действует эта сила
) есть предел отношения нормальной составляющей силы к площади, на которую действует эта сила
В расчетные соотношения термодинамики входит лишь абсолютное давление, определяемое как сумма манометрического (избыточного) давления (pман. ) и давления окружающей среды (p0 ).
В термодинамике для измерения температур используется международная стоградусная температурная шкала Цельсия (t, °С), а в качестве параметра состояния используется абсолютная температура (T, K).
Абсолютная температура(Т) измеряется по термодинамической абсолютной шкале температур, которая аналитически строится на основе дифференциальных соотношений термодинамики. При практическом построении термодинамической шкалы в качестве реперных точек принимаются абсолютный нуль (-273, 15 °С) и параметры тройной точка воды. Между температурами по шкале Кельвина и шкале Цельсия существует следующая зависимость: T = t + 273, 15, К.
|
|
|
|
|
|


