 |
Термодинамические процессы. Термодинамическая работа. Потенциальная (техническая) работа
|
|
|
|
Термодинамические процессы
Изменение состояния системы называется процессом.
Равновесный процесс - это непрерывная последовательность равновесных состояний системы.
Обратимым процессом называется такой равновесный процесс, который в условиях изолированнщй системы допускает возможность возврата этой системы из конечного состояния в исходное путем обратного процесса. В результате прямого и обратного обратимых процессов в системе не происходит каких либо остаточных конечных изменений.
Термодинамическим процессом принято считать обратимый равновесный процесс.
Любой реальный процесс является в большей или меньшей степени неравновесным. Однако, в принципе, эта неравновесность может быть сделана сколь угодной малой в результате уменьшения скорости осуществления процесса. Таким образом, равновесный процесс является предельным случаем неравновесного процесса при стремлении скорости этого процесса к нулю.
Обратимые процессы простых систем могутбыть изображены графически на диаграммах состояния p-v, р-Т и т. д. Линия, изображающая изменение параметров в процессе, называется кривой процесса. Каждая точка кривой процесса характеризует равновесное состояние системы.
Термодинамическая работа
Элементарная термодинамическая работа простых тел – работа обратимого изменения объема определяется в зависимости от величины давления и изменения объема (рис. 1. )
δ L = pdV (1. 5)
Разделив правую и левую часть уравнения (1. 5) на массу G получим выражение для определения удельной элементарной термодинамической работы обратимого изменения объема 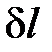 (Дж/кг)
(Дж/кг)
|
|
|
 . (1. 6)
. (1. 6)
Поскольку термодинамическая работа зависит от пути (вида) процесса, для вычисления интегральных значений полной ( 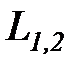 ), или удельной (
), или удельной (  ) работы должны быть заданы уравнения процессов изменения состояния тела в форме,
) работы должны быть заданы уравнения процессов изменения состояния тела в форме, 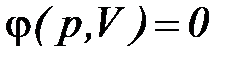 либо его графическое изображение в диаграммах состояния р–V или р–v.
либо его графическое изображение в диаграммах состояния р–V или р–v.
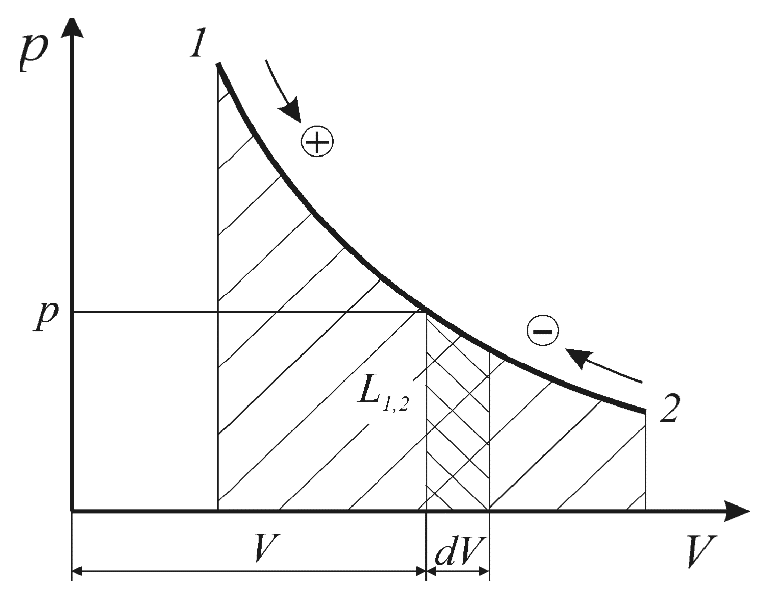
Рис. 1. 1 Термодинамическая работа обратимого изменения объема
Как следует из соотношений (1. 5) работа определяется площадью под кривой процесса и осью ординат независимо от вида рабочего тела и его свойств (рис. 1). В силу этого координаты р–V и р–v называются универсальными координатами работы.
В частном случае для изобарного процесса (p = idem) интегральные значения полной и удельной термодинамической работы определяются по следующим соотношениям:
L1, 2 = 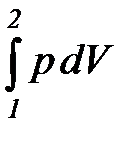 =
=  ; (1. 7)
; (1. 7)
l1, 2 = 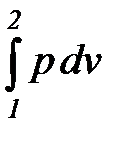 =
= 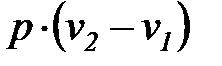 . (1. 8)
. (1. 8)
Работа расширения считается положительной т. е. работа отводится от системы ( 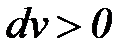 ,
, 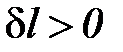 ), а работа сжатия – отрицательной т. е. работа подводится к системе (
), а работа сжатия – отрицательной т. е. работа подводится к системе (  ).
).
Эффективная удельная элементарная работа реального процесса 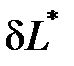 равна разности обратимой работы
равна разности обратимой работы  и работы необратимых потерь
и работы необратимых потерь 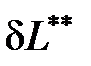 (
( 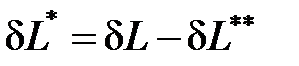 ). Необратимые потери термодинамической работы (
). Необратимые потери термодинамической работы (  ) превращается в теплоту внутреннего теплообмена (
) превращается в теплоту внутреннего теплообмена (  ).
).
Потенциальная (техническая) работа
Потенциальной (технической) работой называется работа по перемещению сплошных масс (газа, пара или жидкости) из области одного давления (p1) в область другого давления (p2), т. е. потенциальная работа - это работа обратимого изменения давления.
Элементарная потенциальная работа простого тела определяется из соотношения
 . (1. 9)
. (1. 9)
Удельная потенциальная работа в элементарном процессе 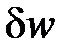 определяется по формуле
определяется по формуле
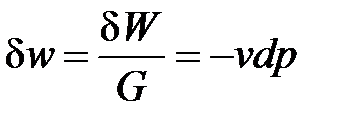 . (1. 10)
. (1. 10)
|
|
|
Для определения интегральных значений полной ( 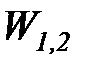 ) или удельной (
) или удельной (  ) потенциальной работы должны быть заданы уравнения процесса изменения состояния рабочего тела
) потенциальной работы должны быть заданы уравнения процесса изменения состояния рабочего тела  или его графическое изображение в диаграммах состояния р–V или р–v.
или его графическое изображение в диаграммах состояния р–V или р–v.
Как следует из соотношений (1. 9), (1. 10), работа определяется в координатах р–V площадью между кривой процесса и осью абсцисс независимо от вида рабочего тела и его свойств (рис. 1. 2).

Рис. 1. 2. Потенциальная работа обратимого изменения давления
В частном случае для изохорного процесса (v = idem) интегральные значения полной и удельной потенциальной работы определяются по следующим соотношениям:
 ;
;  . (1. 11)
. (1. 11)
Потенциальная работа считается положительной при снижении давления (  ) т. е. тработа отводится от системыи отрицательной – при повышении давления (
) т. е. тработа отводится от системыи отрицательной – при повышении давления ( 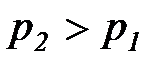 ) т. е. работа подводится к системе.
) т. е. работа подводится к системе.
Эффективная элементарная работа реального процесса  равна разности обратимой работы
равна разности обратимой работы  и работы необратимых потерь
и работы необратимых потерь  (
(  ). Необратимые потери термодинамической работы (
). Необратимые потери термодинамической работы (  ) превращается в теплоту внутреннего теплообмена (
) превращается в теплоту внутреннего теплообмена (  ).
).
Термодинамическая работа (  ) простого тела в замкнутом пространстве и потенциальная работа (
) простого тела в замкнутом пространстве и потенциальная работа (  ) потока непосредственно передаются внешней системе (
) потока непосредственно передаются внешней системе (  или
или 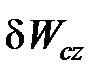 ) и используются для изменения энергии внешнего положения тела (dEcz)
) и используются для изменения энергии внешнего положения тела (dEcz)
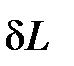 =
=  + dEcz;
+ dEcz; 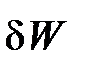 =
= 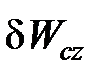 + dEcz . (1. 12)
+ dEcz . (1. 12)
В условиях механических процессов (dEcz=G× cЕ× dcЕ+G× g× dz) уравнение распределения термодинамической и потенциальной работ формулируется следующим образом:
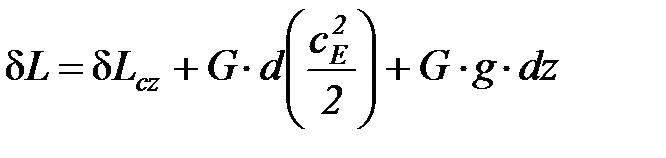 ; (1. 13)
; (1. 13)
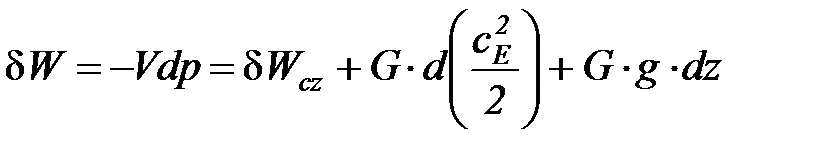 , (1. 14)
, (1. 14)
где cE – скорость движения тела, dz – изменение высоты центра тяжести тела в поле тяготения.
В реальных процессах уравнение распределения термодинамической и потенциальной работ формулируется следующим образом:
 (1. 14а)
(1. 14а)
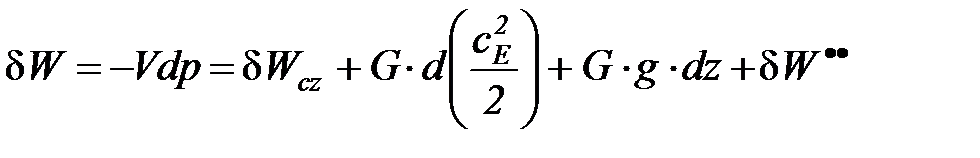 (1. 14б)
(1. 14б)
|
|
|


