 |
Классификация термодинамических процессов
|
|
|
|
Классификация термодинамических процессов
Термодинамический процесс может быть задан либо графическим способом в виде изображения процесса в координатах p-v, p-T, Т-s, либо в аналитической форме в виде зависимости  .
.
Уравнение процесса может быть также задано исходным условием о неизменном значении в этом процессе какой - либо функции состояния (  ) или условием о равенстве нулю какого – либо эффекта термодинамического процесса
) или условием о равенстве нулю какого – либо эффекта термодинамического процесса  , однако и в этом случае исходное условие приводится к основной форме уравнения процесса.
, однако и в этом случае исходное условие приводится к основной форме уравнения процесса.
При изучении термодинамических процессов определяются:
1) закономерность изменения параметров состояния рабочего тела, то есть выводится уравнение процесса или дается его графическое изображение в координатах p-v, p-T, Т-s и т. д.;
2) параметры состояния системы в начальной и конечной точках процесса;
3) численные значения работы и теплообмена в процессе;
4) изменение значений внутренней энергии, энтальпии и энтропии рабочего тела.
Простейшие термодинамические процессы
Простейшими термодинамическими процессами обычно считают изобарный, изохорный и изопотенциальные процессы.
Изобарный процесс ( 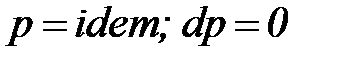 ) – процесс в котором давление в системе остается постоянным.
) – процесс в котором давление в системе остается постоянным.
Изобарный процесс (или изобара) графически представлен на рис. 5.

Рис. 1. 5. Графическое представление изобарного процесса.
В изобарных процессах происходит увеличение (1-2) или уменьшение удельного объема, что связано изменением температуры, обусловленным подводом или отводом теплоты.
Изобарные процессы подвода или отвода теплоты происходят в поршневых двигателях внутреннего сгорания, газотурбинных, паросиловых, холодильных установках и др.
|
|
|
Для идеального газа в изобарном процессе (1-2) значение удельного объема прямо пропорционально температуре рабочего тела 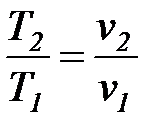 .
.
Удельная термодинамическая и потенциальная работы в изобарном процессе определяются из соотношений
 ,
,  (1. 67)
(1. 67)
В случае идеального газа в силу 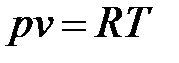 имеем
имеем
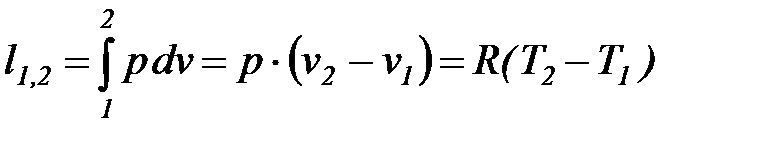 (1. 68)
(1. 68)
Количество теплоты, подведенной к рабочему телу или отведенной от него в изобарном процессе, определяется из выражения первого начала термодинамики
 . (1. 69)
. (1. 69)
Изохорный процесс ( 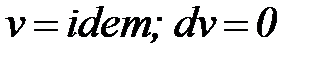 ) – процесс, при котором объем системы или удельный объем рабочего тела остается постоянным (рис. 6).
) – процесс, при котором объем системы или удельный объем рабочего тела остается постоянным (рис. 6).
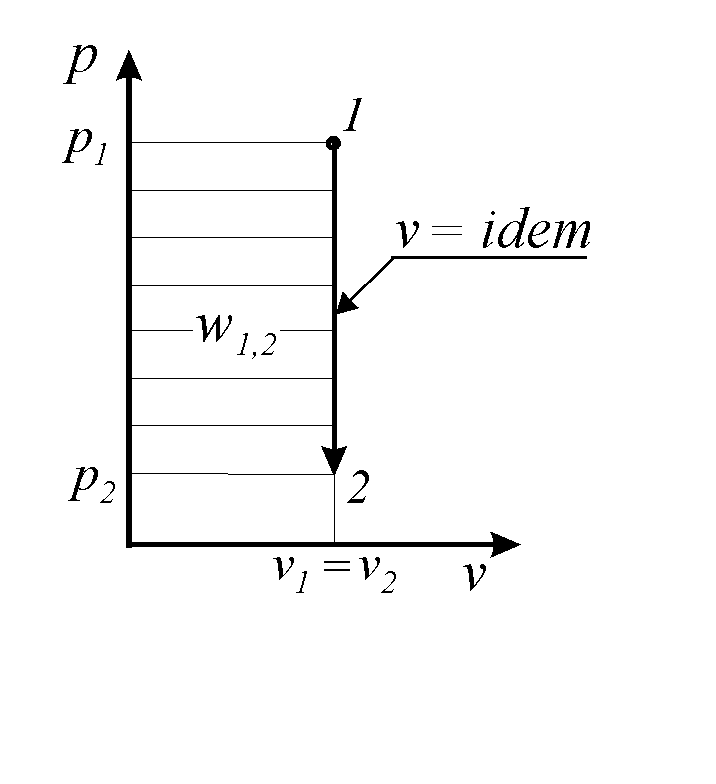
Рис. 1. 6. Графическое представление изохорного процесса.
В изохорных процессах происходит уменьшение (1-2) или увеличение давления, что связано с соответственным изменением температуры – подводом или отводом теплоты.
Изохорные процессы подвода или отвода теплоты происходят в поршневых двигателях внутреннего сгорания, газотурбинных, паросиловых установках и др.
Для идеального газа в изохорном процессе (1-2) давление прямо пропорционально температуре рабочего тела  .
.
Удельная термодинамическая и потенциальная работы в изохорном процессе определяются из соотношений
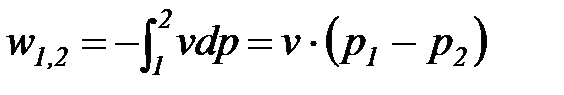
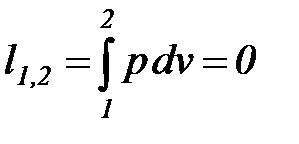 . (1. 70)
. (1. 70)
В случае идеального газа в силу 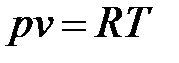 имеем
имеем
 . (1. 71)
. (1. 71)
Количество теплоты, подведенной к рабочему телу или отведенной от него в изохорном процессе, определяется из выражения первого начала термодинамики
 . (1. 72)
. (1. 72)
Изопотенциальный процесс – термодинамический процесс измене-
ния состояния системы, при котором значение потенциальной функции (  ) сохраняет неизменное значение. Для идеального газа, согласно уравнению Клапейрона (
) сохраняет неизменное значение. Для идеального газа, согласно уравнению Клапейрона (  ), изопотенциальный процесс является и изотермическим (
), изопотенциальный процесс является и изотермическим ( 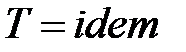 ) (рис. 1. 7).
) (рис. 1. 7).
|
|
|

Рис. 1. 7. Графическое представление изопотенциального
процесса.
Удельная термодинамическая и потенциальная работы в изопотенциальном процессе (1-2) определяются из следующих соотношений:
 =
= 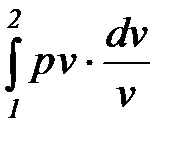 =
=  ; (1. 73)
; (1. 73)
 =
=  =
=  =
=  . (1. 74)
. (1. 74)
Нетрудно заметить, что постоянство потенциальной функции (  ) приводит к равенству логарифмов в выражениях (1. 73) и (1. 74) в силу того, что соблюдается условие
) приводит к равенству логарифмов в выражениях (1. 73) и (1. 74) в силу того, что соблюдается условие  . Поэтому, в изопотенциальном процессе численные значения термодинамической и потенциальной работ равны между собой.
. Поэтому, в изопотенциальном процессе численные значения термодинамической и потенциальной работ равны между собой.
Количество теплоты, подведенной к рабочему телу или отведенной от него в изопотенциальном процессе определяется из выражения первого начала термодинамики по балансу рабочего тела
 . (1. 75)
. (1. 75)
Адиабатический процесс – термодинамический процесс измене-
ния состояния системы, при котором теплообмен равен нулю ( 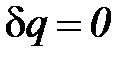 ) и, в силу обратимости процесса, энтропия остается величиной постоянной
) и, в силу обратимости процесса, энтропия остается величиной постоянной
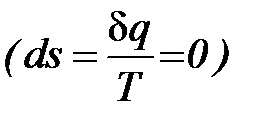 , таким образом адиабатический процесс является и изоэнтропийным (рис. 1. 8).
, таким образом адиабатический процесс является и изоэнтропийным (рис. 1. 8).
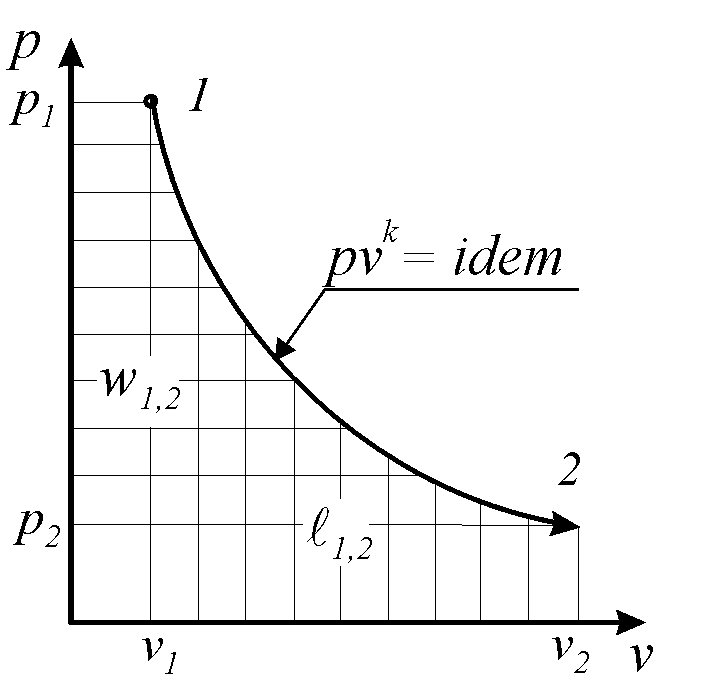
Рис. 1. 8. Графическое представление адиабатического
процесса.
Уравнение и показатель адиабатического процесса может быть получено из выражения первого начала термодинамики для простого тела. При условии, что теплообмен равен нулю имеем:
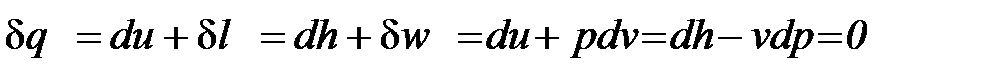 (1. 76)
(1. 76)
Разделяя переменные получим выражение для определения показателя адиабатического процесса
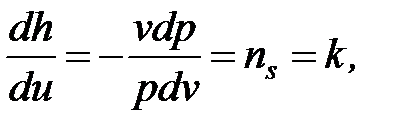
(1. 77)
где ns=k – показатель адиабаты.
Расчетное выражение для расчета показателя адиабатного процесса
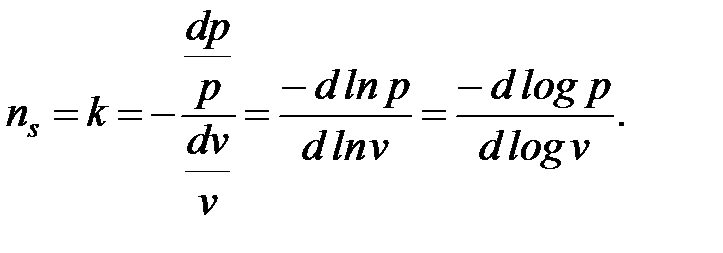
(1. 78)
После интегрирования при условия постоянства показателя процесса имеем
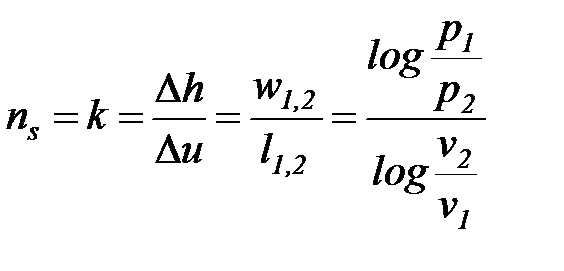
(1. 79)
Для идеального газа показатель адиабаты равен k= cp/cv.
Уравнения перечисленных простейших и любых других термодинамических процессов могут быть представлены одним уравнением. Это уравнение называется уравнением политропы, а термодинамические процессы, описываемые этим уравнением, называются политропными.
|
|
|


